
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
- •Введение
- •Химия воды
- •Понятие о растворах. Процесс растворения. Растворимость веществ
- •Решение типовых задач
- •Задачи для самостоятельной работы
- •Количественная характеристика состава раствора
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.3. Электролитическая диссоциация. Степень и константа диссоциации
- •Задачи для самостоятельного решения
- •1.4. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации
- •Задачи для самостоятельного решения
- •1.5. Диссоциация воды. Водородный показатель
- •Задачи для самостоятельного решения
- •1.6. Гидролиз солей
- •I. Соли, образованные сильным основанием и слабой кислотой
- •II. Соли, образованные слабым основанием и сильной кислотой
- •III. Соли, образованные слабым основанием и слабой кислотой
- •Задачи для самостоятельного решения
- •1.7. Коллоидные растворы
- •Контрольные вопросы
- •1.8. Окислительно-восстановительные реакции
- •Задачи для самостоятельного решения
- •2. Физические и химические свойства технологических процессов водоподготовки
- •2.1. Физико-химическая характеристика природных вод
- •2.2. Физические, химические, биологические показатели качества воды
- •Физико-химические основы коагулирования примесей воды
- •2.4. Коагулянты и флокулянты применяемые для осветления воды
- •2.5. Обеззараживание воды
- •Хлорирование воды.
- •2.5.2. Озонирование воды
- •2.5.3. Применение сильных окислителей и сорбентов. Осаждение
- •2.6. Характеристика бытовых и производственных сточных вод
- •Тест №1
- •3. Микробиология
- •3.1. Основы общей микробиологии
- •3.2. Морфологическая характеристика отдельных групп микроорганизмов
- •1) Меноидный слой с выступами и бугорками; 2) ликополисахаридный слой; 3) каналы; 4) молекулы белка; 5) плотный гликопептидный слой; 6) цитоплазматическая мембрана
- •8) Капсула; 9) мембрана протопласта.
- •3.3. Питание бактерий
- •3.4. Ферменты
- •3.5. Химический состав бактерий
- •3.6. Участие микроорганизмов в круговороте веществ в природе
- •3.7. Водоросли, грибы, простейшие, коловратки, черви и микробактерии
- •5) Surirella saxonica (образование ауксоспор); 6) Asterionella gracillima; 7) Pleurosigma attenuatum; 8) Didymosphenia geminata
- •3.8. Влияние внешних факторов на микробов
- •Тест №2
- •4. Санитарная микробиология
- •4.1. Санитарно-бактериологические методы анализа воды
- •4.2 Физические и физико-химические показатели состава воды
- •4.3. Химические и биохимические показатели
- •Примеси в коллоидном и твердом состояниях
- •Общая минерализация и общая загрязненность воды
- •Примеси в растворенном и коллоидном состояниях
- •Щелочность. Углекислотное равновесие воды
- •Тест №3
- •4.4. Индикаторная роль бактерий группы кишечной палочки
- •5. Биологические факторы самоочищения водоемов
- •6. Вредная деятельность микроорганизмов в системах водоснабжения
- •Тест №4
- •7. Сточные воды и методы их очистки
- •7.1. Очистные сооружения
- •11) Песчаные фильтры; 12) хлораторная; 13) контактный резервуар.
- •7.2. Сооружения механической очистки
- •7.3. Сооружения для биологической очистки.
- •7.4. Аэробные процессы очистки сточных вод
- •7.5. Анаэробные процессы очистки сточных вод
- •7.6. Биологические пруды
- •Тест № 5
- •Заключение
- •Библиографический список
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
Министерство образования и науки РФ
Федеральное государственное бюджетное образовательное учреждение
высшего образования
«Воронежский государственный архитектурно-строительный университет»
Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
Составители:
В.Ф. Бабкин
В.Н. Яценко
Е.П. Евсеев
В оронеж
2016
оронеж
2016
УДК 543.2(07)
ББК 24.46я73
Х465
Рецензенты:
В.Ф. Селеменев д.х.н., проф., заведующий кафедрой аналитической химии Воронежского государственного университета;
Ю.Н. Шалимов д.т.н., проф. кафедры электромеханических систем и электроснабжения Воронежского государственного технического университета
Х465 |
ISBN 978-5-89040-598-2
|
Даются практические теоретические сведения по курсу «Химия воды и микробиологии». По каждому рассматриваемому разделу дисциплины приводятся примеры решения типовых задач, а также задания для самостоятельного решения и тесты для самоконтроля.
Предназначено как для самостоятельной подготовки, так и для проведения аудиторных занятий студентов, обучающихся по профилю 270112 «Водоснабжение и водоотведение».
Ил. 29. Табл. 9. Библиогр.: 6 назв.
УДК 543.2(07)
ББК 24.46я73
Печатается по решению учебно-методического совета
Воронежского ГАСУ
ISBN 978-5-89040-598-2 |
© |
Бабкин В.Ф., Яценко В.Н., Евсеев Е.П., составление, 2016 |
|
© |
Воронежский ГАСУ, 2016 |
Введение
Целью изучения курса «Химия воды и микробиология», является необходимость формирования у студентов знаний об основных характеристиках природных и сточных вод, а также об основных химических, физико-химических и биологических аспектов очистки воды различного назначения.
В процессе обучения наибольшее внимание уделяется теоретической и практической подготовке будущих специалистов по водоснабжению и водоотведению, умению рассчитывать дозы и концентрации реагентов, необходимых для очистки воды, умению классифицировать и рассчитывать растворимость, концентрацию, дозы коагулянта, необходимые при очистке различных типов воды.
Химия воды
Понятие о растворах. Процесс растворения. Растворимость веществ
Растворы — гомогенные (однородные) системы, состоящие из двух или нескольких компонентов и продуктов их взаимодействия
Растворы могут быть жидкие, газообразные, твердые.
Жидкие
растворы
— например раствор поваренной соли
 в воде, раствор азотистой кислоты в воде
и т.д.
в воде, раствор азотистой кислоты в воде
и т.д.
Газообразные
растворы
— например воздух
 других газов.
других газов.
Твердые
растворы
— например сплавы медь + никель:
 ;
;
никель
+ серебро:
 .
.
Наиболее распространенными являются жидкие растворы.
Есть вещества хорошо растворимые, другие — плохо. При растворении веществ могут образовываться насыщенные и ненасыщенные растворы.
Насыщенный раствор — содержит максимальное количество растворяемого вещества при данной температуре.
Ненасыщенный раствор — раствор, в котором еще может растворяться растворяемое вещество при данной температуре.
Пересыщенный раствор — раствор, в котором при данной температуре растворено вещества больше, чем может раствориться.
Растворимость вещества зависит от природы растворителя, от природы растворяемого вещества, температуры, давления (для газов).
Растворимость газов при увеличении давления — увеличивается, а при увеличении температуры, снижается.
На рис. 1 приведена зависимость растворимости твердых веществ от температуры (кривые растворимости).
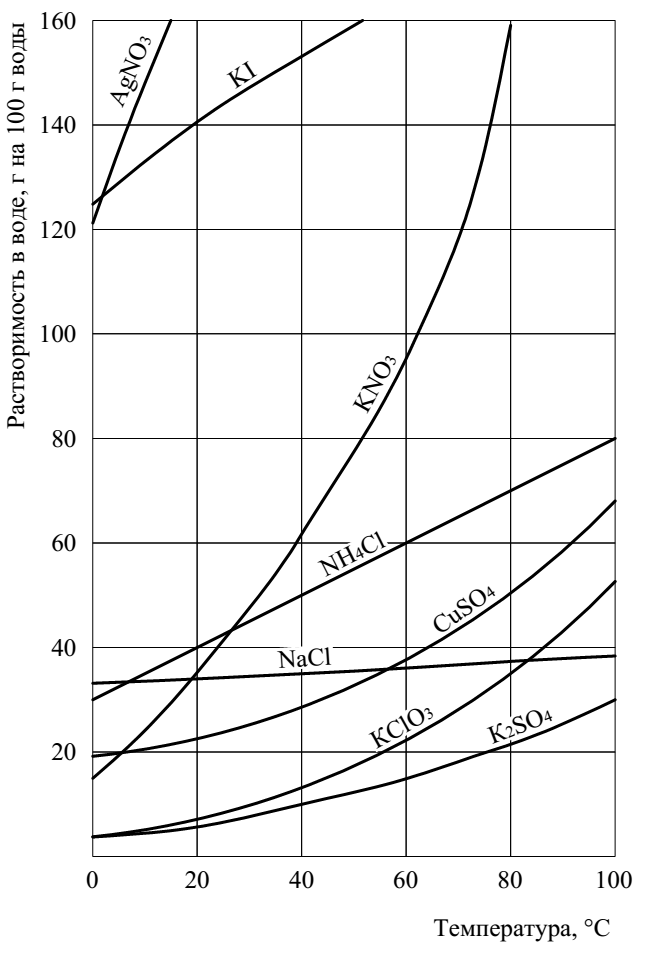
Рис. 1. Кривые растворимости твердых веществ
