
5307
.pdfМИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение высшего образования «Нижегородский государственный архитектурно-строительный университет»
С.В.Митрофанова, И.Л.Смельцова
ХИМИЧЕСКИЕ ЕДИНИЦЫ
КОЛИЧЕСТВА ВЕЩЕСТВА
Учебно-методическое пособие
по подготовке к лекциям, практическим работам и выполнению лабораторных работ (включая рекомендации обучающимся по организации самостоятельной работы) по дисциплине «Химия» для обучающихся по направлению подготовки 05.03.06 Экология и природопользование, направленность (профиль) Прикладная экология и природопользование
Нижний Новгород
2022
2
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение высшего образования «Нижегородский государственный архитектурно-строительный университет»
С.В.Митрофанова, И.Л.Смельцова
ХИМИЧЕСКИЕ ЕДИНИЦЫ
КОЛИЧЕСТВА ВЕЩЕСТВА
Учебно-методическое пособие
по подготовке к лекциям, практическим работам и выполнению лабораторных работ (включая рекомендации обучающимся по организации самостоятельной работы) по дисциплине «Химия» для обучающихся по направлению подготовки 05.03.06 Экология и природопользование, направленность (профиль) Прикладная экология и природопользование
Нижний Новгород
ННГАСУ
2022
3
Митрофанова С.В. Химические единицы количества вещества [Текст]: учеб. - метод. пос. / С.В. Митрофанова, И.Л. Смельцова; Нижегородский государственный архитектурно-строительный университет. – Нижний Новгород: ННГАСУ, 2022. – 19 с. – Текст электронный.
Рассмотрены единицы количества веществ, используемых в химии - углеродная единица, моль и эквивалент, а также производные от них - молярная и эквивалентная масса. Предложены лабораторные работы по экспериментальным методам определения молярной массы веществ, и эквивалентной массы металлов и солей.
Предназначено для обучающихся в ННГАСУ |
по дисциплине «Химия» для |
подготовке к |
|
лекциям, практическим работам и выполнению лабораторных работ (включая |
рекомендации |
||
обучающимся по организации самостоятельной работы) по дисциплине |
«Химия» для |
||
обучающихся по направлению |
подготовки |
05.03.06 Экология и природопользование, |
|
направленность (профиль) Прикладная экология и природопользование
© С.В.Митрофанова,
И.Л. Смельцова, 2022
© ННГАСУ, 2022.
4
Введение Материальная система обладает бесконечным множеством различных
свойств, которые описываются количественными и качественными параметрами.
Некоторые из этих свойств прямо пропорциональны количеству вещества. К ним относятся: масса - мера гравитации и инерции; объем и число структурных элементов, составляющих вещество (молекулы, атомы, электроны и другие частицы). Эти свойства называют экстенсивными. Остальные свойства -
интенсивные. Они не зависят от количества вещества. Например, плотность,
давление, температура и другие.
Количества вещества системы выражают через величины экстенсивных свойств. В практике в качестве единицы количества вещества используют величины массы и объема. В химии и атомной физике единицами количества вещества служат углеродная единица, моль и эквивалент.
Углеродная единица равна 1/12 части массы атома изотопа углерода 12С. В
соответствии с этим массу атомов и молекул, выраженную в углеродных единицах называют относительной атомной и молекулярной массой (так масса атома водорода равна 1,00797 углеродной единицы, масса атома кислорода - 15,9994
углеродной единицы).
Единица количества вещества «моль» связана с числом структурных элементов. Моль - это такое количество вещества, в котором содержится столько структурных элементов (например, молекул, атомов) сколько атомов содержится в
12 г изотопа углерода 12С. В 12 г этого изотопа содержится 6,02 1023 атомов (число Авогадро).
1023 атомов (число Авогадро).
Единица количества вещества «эквивалент» является функцией числа структурных элементов и валентности атомов, образующих это вещество.
Определение эквивалента вытекает из закона эквивалентов: количества вещества,
выраженные в эквивалентах, для всех участников данной химической реакции одинаково. Например, для реакции А + В = С + D 5 эквивалентов вещества А взаимодействует с 5 эквивалентами вещества В и при этом образуется по 5
эквивалентов веществ С и D.

|
5 |
В общем случае: |
= , |
где: m - масса вещества, вступившего в реакцию,
Э - эквивалентная масса вещества.
Эквивалент - это такое количество вещества, которое взаимодействует с 1
эквивалентом водорода. Эквивалент водорода это такое его количество, в котором содержится 6,02.1023 атомов.
Масса и количества вещества, выраженное в молях и эквивалентах, связаны
между собой уравнениями: |
|
m = M . |
(1) |
m = Э . n , |
(2) |
где: m - масса вещества; |
|
- количество вещества в молях;
n - количество вещества в эквивалентах;
М - молярная масса вещества;
Э - эквивалентная масса вещества.
Молярная масса М выражается в единицах г/моль, а эквивалентная Э в г/экв.
Нетрудно найти связь между эквивалентной и молярной массой вещества из формул (1) и (2):
Э = М . / n |
(3) |
Отношение / n обратно пропорционально произведению числа атомов или ионов на их валентность. Найдем эквивалентную массу кислорода: молярная масса кислорода равна 32 г/моль, молекула кислорода состоит из двух атомов,
валентность кислорода равна 2, тогда, Э = М . 1/ 2.2 = 32 . 1/ 4 = 8 г/экв.
Таким образом, эквивалентную массу простого вещества можно рассчитать по формуле:
М вещества
Э простого вещества = |
(4) |

6
Число атомов . Валентность элемента
Очевидно, что эквивалентная масса веществ, образованных атомами,
проявляющими постоянную валентность, постоянна. Например, ЭН= 1 г/экв, ЭО= 8 г/экв, ЭАl= 9 г/экв.
Понятия эквивалента и эквивалентной массы распространяется и на сложные вещества. Эквивалентная масса сложного вещества равна сумме эквивалентных масс простых веществ или ионов, образующих это вещество.
Например, ЭAl2O3 = ЭAl + ЭО = 9 г/экв + 8 г/экв = 17 г/экв;
ЭН2SO4 = ЭН+ + ЭSO42- |
= 1 г/экв + 48 г/экв = 49 г/экв. |
Эквивалентные массы сложных веществ можно рассчитать по следующим |
|
формулам: |
|
Мкислоты |
|
Экислоты = |
(5) |
Число атомов водорода в формуле
Моснования
Эоснования = |
(6) |
Число групп (ОН-) в формуле
Мсоли
Эсоли = |
(7) |
Число атомов металла . Валентность металла
Моксида
Эоксида = |
(8) |
Число атомов элемента . Валентность элемента
Например, молярная масса серной кислоты 98 г/моль, число атомов водорода равно 2, поэтому 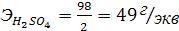
7
Лабораторная работа №1. Определение молярной массы газов.
Цель работы: определить молярную массу одного из газов - воздуха или диоксида углерода (углекислого газа).
Молярную массу газов вычисляют с помощью уравнения Менделеева-
Клапейрона:
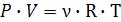 ,
,
где: Р - давление газа (Па, атм или мм рт.ст.);
V - объем газа (м3, л или мл);
- количество вещества в молях;
Т- температура (К);
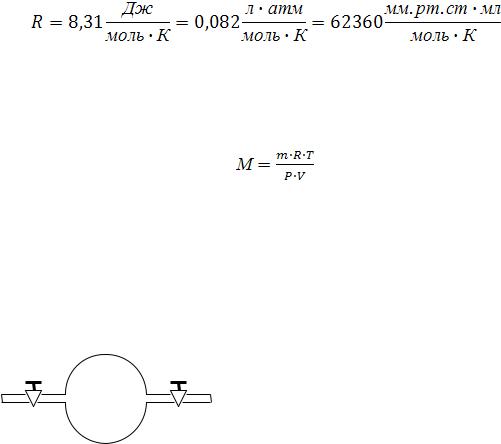
R - универсальная газовая постоянная
Для расчетов выбираете наиболее удобные единицы. Отсюда:
(9)
Экспериментальная часть.
1. Из сосуда, изображенного на рисунке 1, откачивают воздух. Для этого
|
|
сосуд, изображенный на рисунке 1, соединяют |
|
|
резиновым шлангом с вакуумным насосом. |
|
|
При открытом кране 1 и закрытом кране 2 |
1 |
2 |
включить насос на 2-3 минуты. Закрыть кран |
Рис. 1. Сосуд для определения |
1, отсоединить сосуд от насоса. |
|
|
||
молярной массы газа.
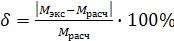
8
2.Вакуумированный сосуд осторожно взвешивают на технических весах с точностью 0,01 г. Записать массу сосуда m1.
3.Для заполнения сосуда воздухом осторожно открыть краны 1 и 2. Для заполнения сосуда углекислым газом, его с помощью резинового шланга присоединяют к аппарату Киппа, осторожно открывают краны 1 и 2, открывают кран на аппарате Киппа и медленно пропускают СО2. При этом заполняемый сосуд располагают вертикально и СО2 подают снизу.
4.Взвешивают сосуд, заполненный газом на технических весах. Записать массу сосуда m2 и по разности m2 - m1 найти массу газа.
5.Определяют значения комнатной температуры и атмосферного давления.
Используя полученные данные:
m1 - масса вакуумированного сосуда; m2 - масса сосуда, заполненного газом;
Р - атмосферное давление (давление газа);
Т – температура.
Молярная масса воздуха равна 29 г/моль.
По уравнению (9) рассчитывают молярную массу газа.
Вычисляют относительную погрешность:
|
, |
|
где: Мэкс. |
- молярная масса газа, вычисленная из экспериментальных |
|
данных; |
|
|
Мрасч. |
- молярная масса газа, рассчитанная на основании |
|
относительных атомных масс. |
|
|
|
ВЫВОД |
|
1. Получено экспериментальное значение молярной массы |
............(воздуха или |
|
СО2), равное .................... |
г/моль. |
|
2. Относительная ошибка измерения составила ................................. |
%. |
|
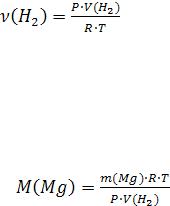
9
Лабораторная работа №2.
Определение молярной массы металла.
Цель работы: экспериментальным путем определить молярную массу магния.
В основе одного из экспериментальных методов определения молярной массы металлов, вытесняющих из кислот водород, лежит реакция между навеской металла и избытком кислоты.
Mg + 2 HCl = MgCl2 + H2
При растворении двухвалентного металла число молей, выделившегося водорода, равно числу молей растворившегося металла. Измерив объем выделившегося водорода, его давление и температуру вычисляют число молей выделившегося водорода из уравнения Менделеева-Клапейрона
(10)
ν (H2) = νМg, а из уравнения (1) ММg = mм/ νМg, тогда
Подставив mH2 из уравнения (11) в уравнение (10), получим:
(11)
Экспериментальная часть.
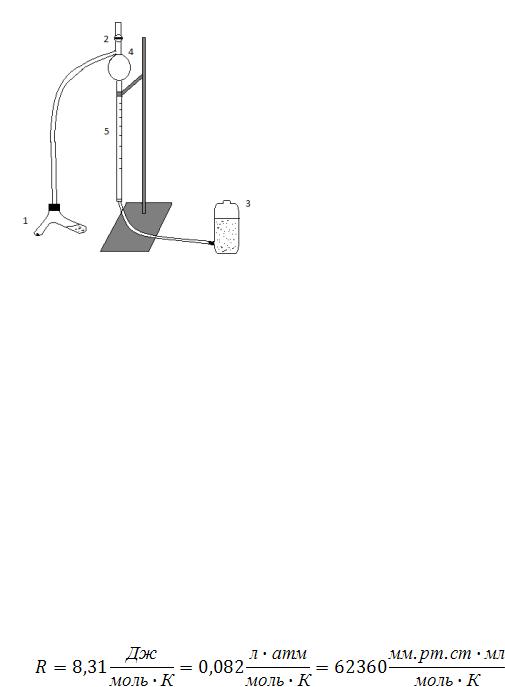
1. В короткое колено сосуда 1, изображенного на рисунке 2, помещают навеску магния, а в длинное колено избыток соляной кислоты (15 мл 13 %
раствора). Сосуд закрываем пробкой с резиновой трубкой, соединяющей сосуд 1 с
измерительной бюреткой 5.
|
10 |
|
|
|
2. |
Открывают кран 2 и с помощью |
|
|
внительной склянки с водой 3 заполняют |
||
|
юретку до метки 4, совместив уровни воды в |
||
|
мерительной склянке и бюретке. Закрывают |
||
|
кран 2. |
|
|
|
3. |
Осторожно приливают кислоту |
к |
|
гнию небольшими порциями. |
|
|
|
4. |
После окончания реакции сосуд 1 |
|
|
лаждают до комнатной температуры и |
||
Рис. 2. Схема установки. |
измеряют объем выделившегося водорода, |
||
|
|
|
|
|
предварительно совместив уровни воды |
в |
|
уравнительной склянке и бюретке.
5. Определяют температуру и атмосферное давление.
Из экспериментальных данных:
mм - масса магния (г),
VH2 - объем выделившегося водорода (л),
Р - атмосферное давление (атм),
Т - температура (К),
R - универсальная газовая постоянная
(для расчетов выбираете наиболее удобные единицы),
по уравнению (11) находят Мм.
Относительную погрешность измерения вычисляют по формуле:
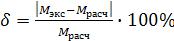 ,
,
где: Мэкс.- молярная масса магния, вычисленная из экспериментальных данных;
Мрасч.- молярная масса магния, рассчитанная по таблице Менделеева.
