

ОБПЩИЕ УТИ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ
Метаболизм представляетсобойвысоко |
координированнуюцеленаправленнуюкл |
е- |
|
точнуюактивность, |
обеспеченнуюучастиеммногвза мосвязанныхферментативных |
и- |
|
стем. |
|
|
|
Онвыполняеттриспециализированныефункции:
1.Энергетическая – снабженклеткхимэнической, ргие
2.Пластическая – синтезмакромкакстроблоковлекулительных,
3. Специфическая – синтез |
распад биом,необходимыхлекулдлявыполнениясп |
е- |
|||
цифическихклеточныхфункций. |
|
|
|
|
|
|
А Н А Б О Л И З М |
|
|
||
Анаболизм – этобиосинтезбелков, |
полисахаридов, |
и- |
|
||
пидов, |
нуклеинкислотдругихмакромолекулвыхизмалых |
|
|
|
|
молекул-предше.Посонсопровождтвенниковкольку |
|
ается |
|
||
усложнениемструктуры,тотребузатратэнергии.Источн |
энергияАТФ |
|
и- |
|
|
комтакойэнергииявляется |
. |
|
|
||
Такжедлябиосиннекоторыхвеществжирныееза( ки |
|
|
с- |
|
|
лоты,холе |
стерол)требуюбогатыеэнергиейатомысяводор |
|
о- |
|
|
да – ихисточникомявляется |
|
НАДФН. Молекулы НАДФН об- |
|
|
||||
разуютсяв |
реакциях |
окисленияглюкозо |
|
-6-фосфата( |
см |
|
|
|
"Пентозофосфатныйпутьокисленияглюкозы |
|
|
|
")иоксалоацетасм(Биосин" жирныхки теза |
|
с- |
||
лот") . В реакциях анаболизма НАДФНпередаетсвоиатомыводородана |
|
синтетическиер |
е- |
|||||
акции окисляетсядоНАДФ. |
|
Такф |
ормируется НАДФ-НАДФН-цикл. |
|
|
|||
|
|
|
|
К А Т А Б О Л И З М |
|
|
|
|
Катаболизм – расщепление иокисление |
сложныхрганическихмолекулдоболеепр |
|
о- |
|||||
стыхконечныхпродуктов.Оносопровождаетсявысвобождениемэнергии,заключенной |
|
|
|
|
|
|||
сложной структуревеществ. |
|
Большаячасть |
высвобожденной энергиирассеиваетсяде |
|
||||
тепла.Меньшаячастьэтой |
|
нергииперехватывается" "коферментамиокислительныхреа |
|
|
к- |
|||
цийНАДФАД,некотораячастьсразуисподсинтляьзуАТФ. езатся |
атомыв |
одорода,высвобреаокждаемыецияхисленияв |
|
|
||||
Следуетзаметить,что |
|
|
е- |
|||||
ществ,могутиспоклтолькоьзоватьсяеткойподвумнаправлениям: |
|
|
|
|
|
|||
1)на |
анаболические реакциивсоставе |
НАДФН. |
|
|
|
|||
2)наобразование |
|
АТФ всоставе НАДН и ФАДН2 вдыхательнойцепи |
митохондрий |
|||||
(смниже). |
|
|
|
|
|
|
|
|
Весь катаболиподрнатриэтапазделяется:м |
|
|
|
|
|
|||
|
|
|
|
Iэтап |
|
|
|
|
Происходитв |
кишечнике (переварил) щивание |
лизосомах прасщеплении |
|
|||||
ужененужныхмолекул.Приэтомосвоколоб1%энергииждается,заключвмолекнной |
|
|
|
|
у- |
|||
ле.Онарассеиваетсявидетепла. |
|
|
|
|
|
|
|
|

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
81 |
|
|
|
II этап
Вещества, образованные при внутриклеточном гидролизе или проникающие в клетку из крови, обычно превращаются в
пировиноградную кислоту, ацетильную группу (в составе ацетил-SКоА), и в некоторые другие мелкие органические молекулы. Локализация второго этапа – цитозоль и митохондрии.
Часть энергии рассеивается в виде тепла и примерно 13% энергии вещества усваивается, т.е. запасается в виде макроэргических связей АТФ.
III этап
Все реакции этого этапа идут в митохондриях. АцетилSКоА включается в реакции
цикла трикарбоновых кислот
и окисляется до углекислого газа. Выделенные атомы водорода
соединяются с НАД и ФАД и восстанавливают их. После этого НАДН и ФАДН2 переносят водород в цепь дыхательных ферментов, расположенную на внутренней мембране митохондрий. Здесь в результате процесса под названием "окислительное фосфорилирование" образуется вода и главный продукт биологического окисления – АТФ.
Часть выделенной на этом этапе энергии молекулы рассеивается в виде тепла и около 46% энергии исходного вещества усваивается, т.е. запасается в связях АТФ и ГТФ.
На втором этапе выделяется около 30% энергии, заключенной в молекуле. При этом запасается около 13% от всей энергии вещества (или примерно 43% от выделенной на этом этапе энергии).
В третьем этапе выделяется до 70% всей энергии вещества. Из этого количества усваивается почти две трети (66%), что составляет около 46% от общей.
Таким образом, из 100% молекулярной энергии клетка запасает больше половины
– 59%. Ни один современный двигатель не имеет такого высокого КПД!

Общпутиологичеокисленияского |
82 |
|
|
Энергия,высвобождреакцияхкатабол,з паемаяввидесвязейзма,называтся |
е- |
мых макроэргическими.Основнойиуниверсальноймолекулой,запасающейэнергию,я |
в- |
ляется АТФ. |
|
ВсемолекулыАТФворганизменепрерыучаствкакихвуютно |
|
-либореакциях, |
посто- |
яннорасщепляютсядоАДФивновьрегенерируют.Существуеттриосновныхспособа |
|
|
с- |
пользАТФ,ковторыекупеания |
спроцессбразА омвания |
ТФ получилиназвание |
АТФ- |
цикл. |
|
|
|
О С НИОС ТВОНЧЫНЕИ К И |
|
|
Э НВЕК РЛГЕИТИКЕ |
|
|
|
|||||
В клеткесущ ствуют |
|
четыре основных процесса,обеспечивающих |
высвобождение |
||||||||
энергии изхимическихсвязей |
|
приокислении |
|
веществ иеезапасание |
: |
|
|
|
|||
1. Гликолиз (2этап) |
– окислениемолекулыглюкозыдодвухмолекул |
|
|
|
пировиноград- |
||||||
нойкислоты |
, приэтом |
образумолекулы2 АТФтся |
|
|
иНАДН . Далеепировинограднаякисл |
|
о- |
||||
та в аэробных условияхпре ацетилращается |
|
-SКоА, в анаэробных условиях – в молочную |
|||||||||
кислоту. |
|
|
|
|
|
|
|
|
|
|
|
2. β-Окислениежирныхкислот |
|
(2этап) |
– окислежиркислотдонацыхиеетил |
|
|
-SКоА, |
|||||
здесьобразуютсямолекулыНАДНиФАДН |
|
|
2. МолекулАТФ |
"вчистомвиде"необразуется. |
ппы (вс |
о- |
|||||
3. Циклтрикислотарбоновых |
(ЦТК ,этап3 |
) – окисление ацетильнойгру |
|||||||||
ставеацетил |
-SКоА) илииныхкетокислот |
доуглекислогогаза |
. Реакции полногоцикла |
|
со- |
||||||
провождаютсяобразованием |
1молекулыГ |
ТФчто(эквивалентно |
|
однойАТФ),молекул3 |
|
|
|||||
НАДНимолекулы1 ФАДН |
|
|
2. |
|
|
|
|
|
ФАДН2, полу- |
||
4. Окислительноефосфорилирование |
|
(3этап) |
– окисляются НАДНи |
||||||||
ченные вреакцияхкатаболизма |
|
глюкозыижирныхкислот.Приэтом |
|
|
|
ферменты внутренней |
|||||
мембраныитохондрий |
обеспечивают образование оснковноголичества |
|
клеточного АТФ |
||||||||
изАДФ (фосфорилирование). |
|
|
|
|
|
|
|
|
|||
ОсновнымспособомполученияАТФклеткеявлокислительноеетсяфосфорилиров |
|
|
|
|
|
|
|
а- |
|||
ние.ОднакотакжеестьдругойспособфосфорилированияАДФдоАТФ |
|
|
|
|
– субстратное фос- |
||||||
форилирование.Этотспособсвязан |
спередачеймакроэргфосфатаилэнергиического |
|
|
|
|
|
|||||
макроэргическойсвязикакого |
|
-либовеществасубстрата( )наАДФ.К |
|
|
|
таким веществамотн |
о- |
||||
сятсяметаболитыгликолиза( |
|
1,3-дифосфоглицериноваякислота |
|
, фосфоенолпируват), |
|||||||

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
83 |
|
|
|
цикла трикарбоновых кислот (сукцинил-SКоА) и креатинфосфат. Энергия гидролиза их макроэргической связи выше, чем в АТФ (7,3 ккал/моль), и роль этих веществ сводится к использованию для фосфорилирования АДФ.
ОК И С Л И Т Е Л Ь Н О Е Д Е К А Р Б О К С И Л И Р О В А Н И Е
ПИ Р О В И Н О Г Р А Д Н О Й К И С Л О Т Ы
Пировиноградная кислота (ПВК, пируват) является продуктом окисления глюкозы и некоторых аминокислот. Ее судьба различна в зависимости от доступности кислорода в клетке. В анаэробных условиях она восстанавливается до молочной кислоты. В аэробных условиях происходит ее окисли-
тельное декарбоксилирование до уксусной кисло-
ты, переносчиком которой служит коэнзим А.
Суммарное уравнение реакции отражает декарбоксилирование пирувата, восстановление НАД до НАДН и образование ацетил-SKoA.
Превращение состоит из пяти последовательных реакций, осуществляется мультиферментным комплексом, прикрепленным к внутренней митохондриальной мембране со стороны матрикса. В составе комплекса насчитывают 3 фермента и 5 коферментов:
Пируватдегидрогеназа (Е1, ПВК-дегидрогеназа), ее коферментом является тиаминдифосфат, катализирует 1-ю реакцию.
Дигидролипоат-ацетилтрансфераза (Е2), ее коферментом является липоевая кисло-
та, катализирует 2-ю и 3-ю реакции.
Дигидролипоат-дегидрогеназа (Е3), кофермент – ФАД, катализирует 4-ю и 5-ю реак-
ции.
Помимо указанных коферментов, которые прочно связаны с соответствующими ферментами, в работе комплекса принимают участие коэнзим А и НАД.
Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется пируватдегидрогеназой, Е1), окислению пирувата до ацетила и переносу ацетила на коэнзим А (катализируется дигидролипоамид-ацетилтрансферазой, Е2).
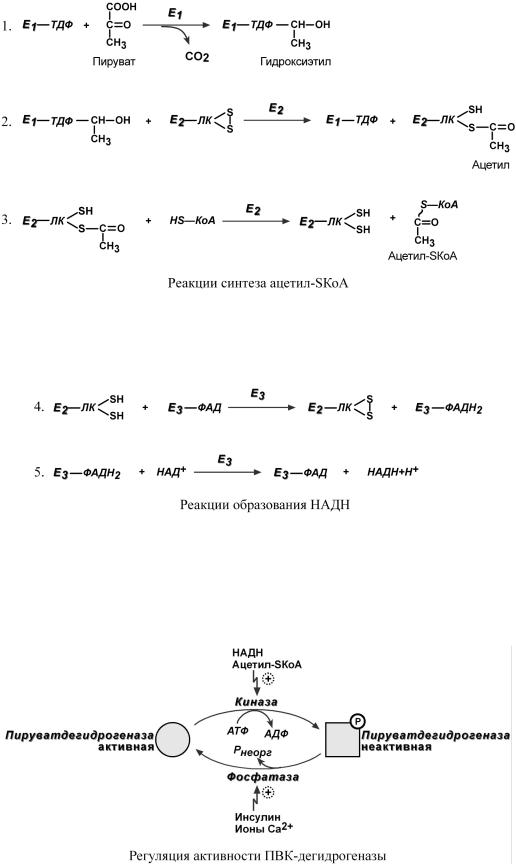
Общпутиологичеокисленияского |
84 |
|
|
Оставшиесяреакции2 необходдлвозвращлипомыкислеФАДвниявокийты |
с- |
|
ленноесостояние( |
катализируются дигидролипоат-дегидрогеназой,Е 3). Приэтомобразуется |
|
НАДН. |
|
|
РЕ Г У Л Я Ц И Я ПИРУВАТДЕГИДРОГЕНАЗНОГОКОМПЛЕКСА |
|
Впируватдегидрогеназномкомплексеимеютсяещевспомогательных2 фермента |
– ки- |
наза и фосфатаза,участвующие регуляцииактивностипируватдегидрогеназы |
(Е 1) путем |
фосфорилирования и дефосфорилирования. |
|
Киназа активируетсяпри |
избытке АТФ ипродуреакциитов |
– НАДН и ацетил-SКоА. |
Приэтомонафосфопируватдегидрогеназуилирует, |
инактивируя ее. |
|

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
85 |
|
|
|
Фосфатаза, активируясь ионами кальция или инсулином, отщепляет фосфат и активирует пируватдегидрогеназу.
Таким образом, в состоянии покоя при достаточном количестве АТФ пируватдегидрогеназа неактивна, окисление глюкозы прекращается, и она может использоваться на какиелибо синтетические процессы. Как только клетка начинает работать, уровень АТФ и НАДН резко снижается, киназная реакция останавливается, и в результате дефосфорилирования фермент активируется – начинается окисление глюкозы.
В головном мозге доля пирувата, поступающая на ПВК-дегидрогеназу, составляет 80-90%, в отличие от печени, где эта доля соответствует 15-20%. В печени ПВК в основном используется для синтеза оксалоацетата. Этим объясняется высокая чувствительность нервной ткани к дефициту тиамина.
Ц И К Л Т Р И К А Р Б О Н О В Ы Х К И С Л О Т
Образующийся в ПВК-дегидрогеназной реакции ацетил-SКоА далее вступает в цикл трикарбоновых кислот (ЦТК, цикл лимонной кислоты, цикл Кребса).
Впервой реакции цикла связываются ацетил и оксалоацетат (щавелевоуксусная кислота) с образованием цитрата (лимонной кислоты), далее происходит изомеризация ли-
монной кислоты до изоцитрата и две реакции дегидрирования с выделением СО2 и восстановлением НАД. В пятой реакции образуется ГТФ, это реакция субстратного фосфорилирования. Последние три реакции представляет собой дегидрирование, гидратацию и новое
дегидрирование субстратов.
Витоге после восьми реакций цикла вновь образуется оксалоацетат.
Функции ЦТК:
1.Энергетическая – заключается в синтезе одной молекулы ГТФ (эквивалентна АТФ) и в генерации атомов водорода для работы дыхательной цепи (см ниже), а именно трех молекул НАДН и одной молекулы ФАДН2;
2.Анаболическая – в ЦТК образуется
o предшественник гема – сукцинил-SКоА,
o кетокислоты, способные превращаться в аминокислоты – α-кетоглутарат для глутаминовой кислоты, оксалоацетат для аспарагиновой,
o лимонная кислота, используемая для синтеза жирных кислот (при определенных условиях),
o оксалоацетат, используемый для синтеза глюкозы (при определенных условиях). Цикл Кребса протекает в матриксе митохондрий и включает 8 реакций. Он представ-
ляет собой последовательные реакции связывания ацетила и щавелевоуксусной кислоты (оксалоацетата) с образованием лимонной кислоты, ее изомеризации и последующие реакции окисления с сопутствующим выделением СО2. После восьми реакций цикла вновь образуется оксалоацетат.

Общпутиологичеокисленияского |
86 |
|
|
|
РЕ Г У Л Я Ц И Я ЦТК |
|
|
1. ГлавиоснрегуляторомовнымЦТКявляется |
оксалоацетат,аточнееего |
до- |
|
ступность.НаличиеоксалоацетаацетилвовЦТКлекает |
-SКоА изапускает процесс. |
|
|
Обычно вклеткеимебалансмеждутсяобрацетилзованием |
-SКоА (изглюкозы,жи |
р- |
|
ныхкислотилиамин)колкоксалоацетатаислотчес. вом |
Источником оксалоацетата яв- |
||
ляетсясинтезизпирувата( |
анаплеротическая или пополняющая реакц),поступлениезя |
|
|
фруктовыхкисл |
отсамогоЦТКяб( л, очнойимонной),образспарагиновойованиекисл |
|
о- |
ты. |
|
|
|

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
87 |
|
|
|
Понимание такого способа регуляции позволяет понять причину синтеза кетоновых тел и кетоацидоза при декомпенсации сахарного диабета I типа и при голодании. При указанных нарушениях в печени активирован процесс глюконеогенеза, т.е. образования глюкозы из оксалоацетата и других метаболитов, что влечет за собой снижение количества оксалоацетата. Одновременная активация окисления жирных кислот и накопление ацетил-SКоА запускает резервный путь утилизации ацетильной группы – синтез кетоновых тел. В организме при этом развивается закисление крови (кетоацидоз) с характерной клинической кар-
Общпутиологичеокисленияского |
|
|
|
|
|
|
|
|
|
|
88 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
тиной:слабость,гол,совльн,снижениеаяливостьмышечноготонуса,температу |
|
|
|
|
|
|
|
|
рытела |
|||||
иартериальногодавления. |
|
|
|
|
|
|
|
|
аллостерической ре- |
|||||
|
2. ТакженекоторыеферментыЦТКявляются |
|
|
|
чувствительнымик |
|||||||||
гуляцииметаболитами |
. |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
Ингибиторы |
|
|
Активаторы |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Цитратсинтаза |
|
|
АТФ,НАДН, |
|
|
|
|
|
|
|
|||
|
|
|
ацил-SКоА, цитрат |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
Изоцитрат-дегидрогеназа |
|
|
АТФ,НАДН |
|
|
|
АМФ,АДФ |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
α-Кетоглутарат-дегидрогеназа |
Сукцинил-SКоА, |
|
|
|
|
|
|
||||||
|
АТФ, |
НАДН |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|||||||||
|
О К И СФЛОИСТФЕОЛРЬ Н О Е |
|
И Л И Р О В А Н И Е |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||
|
Окислительноефосфорилирование |
|
|
– основнаячастьбиологокилисленияческого |
|
|
|
|
||||||
тканевогодыхан,..процессов,идущихяорганизмеучастиемкислорода. |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
К Р А Т К А Я Х А Р А К Т Е Р И С Т И К А |
|
|
|
|
|||||||
|
Окислительноефосфорилирование |
|
|
– этомногоэтапныйпроцесс,проивоходящий |
|
|
|
|
||||||
внутреннеймемитохондрийбране |
|
и заключающийсявокислениивосстаноэквивленных |
|
|
|
|
а- |
|||||||
лентовНАДН( иФАДН |
|
2) исопровождающийсясинтезомАТФ. |
|
|
|
|
|
Питером Мит- |
||||||
|
Впервые механизм окислительногофосфорилировабылпредложения |
|
|
|
||||||||||
челлом в1961г |
.Согласноэтойгипотезе |
|
|
переносэлектронов |
,происходящийнавнутренней |
|
|
|
||||||
митохондмемб,вызываетриальнойане |
|
|
выкачивание ионовН |
+ изматриксамитохондрийв |
|
|
||||||||
межмембранноеп |
ространство.Это |
создает градиент концентрации ионовН |
+ междуцит |
о- |
||||||||||
золем изамкнутымвнутрипростраитохо. ндриальнымством |
|
|
|
|
Ионы водорода внорме |
спо- |
||||||||
собны возвращатьсявматрикс |
митохондрий толькооднимсп собом |
|
|
– черспециальныйз |
|
|
||||||||
фермент,образующийАТФ |
– АТФ-синтазу. |
|
|
|
|
|
|
|
|
|||||
|
Внутренняя митохондмембсодержитрядмуиаанальткомпленаяиферментных |
|
|
|
|
|
|
к- |
||||||
сов,включающихмножествоферм.Этирментытоваздыхательнымиваютфермент |
|
|
|
|
– дыхательнойцепью |
|
|
а- |
||||||
ми,апоследоватихрасположениям мбранельность |
|
|
|
|
|
. |
|
|
||||||
|
|
|
П Р ИРНАЦДБИЫОПХТ АЫТ Е |
|
|
Л ЬЦНЕОПЙИ |
|
|
|
|
||||
|
В целом работадыхцепизаключаетсятельнойвследующем: |
|
НАДН и ФАДН2 передают атомы водорода (т .е. |
|||||||||||
1Образующиеся. |
вреакцияхкатаболизма |
|
||||||||||||
протоны водорода и электроны) на ферменты дыхательной цепи. |
|
|
|
|
||||||||||
2Электроны. движутсяподыхацепитеэнергиюльнойряют. |
|
|
|
|
+ изматриксавмежмембранноепр |
|
|
|
||||||
3. ЭтаэнергияиспользуетсянавыкачивапротоновН ие |
|
|
|
|
|
о- |
||||||||
странство. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4Вконце. дыхательцепиэлектроныпопкислородойадаютвосстанавливаютегодо |
|
|
|
|
|
|
|
|
о- |
|||||
ды. |
+ стремяобратновматипсяиксчерезоходятАТФ |
|
|
|
|
|
|
|
|
|
|
|
||
5Протоны. Н |
|
|
|
|
|
|
-синтазу. |
|
|
|
||||
6При.этомонитеряютэнергию,котораяисподсинтляьзуАТФ. езатся

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
89 |
|
|
|
Ф Е Р М Е Н Т Н Ы Е К О М П Л Е К С Ы Д Ы Х А Т Е Л Ь Н О Й Ц Е П И
Всего цепь переноса электронов включает в себя около 40 разнообразных белков. Все они организованы в 4 больших мембраносвязанных мульферментных комплекса.
I КОМ ПЛЕКС , НАДН-KO Q-ОКСИДОРЕДУКТАЗА
I комплекс носит общее название НАДН-дегидрогеназа, содержит ФМН, белковые молекулы, из них 6 железосерных белков.
Функция
1.Принимает электроны от НАДН и передает их на коэнзим Q (убихинон).
2.Переносит 4 иона Н+ на наружную поверхность внутренней митохондриальной мембраны.
Железосерные белки (FeS-белки) – это белки содержащие атомы железа, связанные с атомами серы. Атомы железа соединены с атомами серы и с серой остатков цистеина, образуя железо-серный центр.
IIКОМ ПЛЕКС
IIкомплекс – как таковой не существует, его выделение условно, он включает в себя ФАД-зависимые ферменты, расположенные на внутренней мембране – например, ацил- SКоА-дегидрогеназа (окисление жирных кислот), сукцинатдегидрогеназа (цикл трикарбоновых кислот), митохондриальная глицерол-3-фосфат-дегидрогеназа (челночный механизм переноса атомов водорода).
Функция
1.Восстановление ФАД в окислительно-восстановительных реакциях.
2.Обеспечение передачи электронов от ФАДН2 на железосерные белки внутренней мембраны митохондрий. Далее эти электроны попадают на коэнзим Q.
