Выберите одну пару утверждений, которые правильно характеризуют самопроизвольную ОВР: 2MnO4 + 5NO2 + 6H+ ; 2Mn2+ + 5NO3 + 3H2O
Eo (MnO4 / Mn2+)=1,51B; Eo (NO3 /NO2 )=0,94B
Стандартный окислительно-восстановительный потенциал системы пируват/лактат при рН=7 составляет - 0,180 В. Выберите верные утверждения:
Расположите растворы в ряд по увеличению потенциала погруженного в них водородного электрода:
|
0,1 н NaOH
|
вода
|
0,1 н HCl
|
Выберите верные утверждения для элемента:
Ag AgCl, KСlнас. физ.раствор (XГ) Pt
EoХГ = 0,699В, Ехс= 0,202В
Гальванический элемент состоит из водородного электрода, погруженного в 0,01н раствор гидроксида натрия, и хингидронного электрода в 0,01 н растворе НCL. Еохг=0,699 В. Выберите верные утверждения для этого элемента:
ЭДС элемента, составленного из насыщенного каломельного электрода и водородного электрода, опущенного в желудочный сок, равна 0,421 В.
Екал = 0,244 В. Рассчитать рН желудочного сока с точностью до целых.
Выберите верные утверждения, характеризующие процесс диссоциации комплексного соединения K3[Fe (CN)6]:
Выберите верные утверждения, характеризующие процесс диссоциации комплексного соединения [Pt (NH3)2 Cl2 ] :
Установите соответствие между комплексным соединением и комплексообразователем в его составе:
комплекс ----------------------------------- комплексообразователь
|
Гемоглобин
|
ион железа
|
Хлорофилл
|
ион магния
|
Mg[Cd (CN)4]
|
ион кадмия
|
Cd[Pt (CN)4]
|
ион платины с зарядом +2
|
Выберите верные утверждения, характеризующие процесс диссоциации комплексного соединения К2[Cd (CN)4] :
Расположите комплексы меди с аспарагином, аланином и глицином в порядке увеличения их устойчивости. Константы нестойкости соответственно равны:
|
1,4*10-8
|
1,2*10-15
|
4*10-18
|
Константы нестойкости комплексов токсичного свинца с биосубстратом в организме и с комплексоном соответственно равны 10-4 и 10-10. Выберите верные утверждения.
Константы нестойкости комплексов :
[Ag(NH3)2]+=10-8
[NH4]+= 10-10
[Pt(NH3)4]+2=10-34
Выберите верные утверждения.
Комплекс серебра можно разрушить сильной кислотой
Комплекс серебра менее устойчив, чем комплекс платины
Даны константы нестойкости комплексов цинка с пиридином и аммиаком соответственно равны : 10-2 и 10-10. Выберите верное утверждение:
К насыщенному раствору хлорида серебра с донной фазой добавили одно из перечисленных веществ. В каких случаях изменится растворимость AgCl:
хлорид натрия
нитрат серебра
этанол
Известно, что этот процесс растворения хлорида натрия эндотермический. Выберите верные утверждения:
Установить последовательность выпадения осадков при добавлении раствора нитрата серебра к раствору, содержащему хлорид-, бромид- и иодид- ионы в равных количествах.
|
ПР(AgI) = 8,3*10-17
|
ПР(AgBr) = 5,3*10-13
|
ПР(AgCl) = 1,8 *10-10
|
Какую соль нужно добавить к раствору сульфида натрия для наиболее эффективного удаления сульфид-ионов – нитрат свинца (II), нитрат ртути (II) или нитрат платины (II) ? Расположите эти соли в порядке уменьшения эффективности
|
ПР(PtS) = 1.2*10-61
|
ПР(HgS) = 1.6*10-52
|
ПР( PbS) = 2.5*10-27
|
При лечении опухолей используются комплексные соединения платины. Используя данные константы, выберите верные утверждения:
ПР (Pt(OH)2) = 10-35, Кнест [PtCl4]2- = 10-43
Можно приготовить лекарство, содержащее [PtCl4]2- , используя свеже-осажденный гидроксид платины (II)
При добавлении ионов хлора осадок Pt(OH)2 растворяется
Концентрация свободных ионов кальция в плазме крови 1,1*10-3 моль/л; гидрофосфат-анионов 2,9*10-4 моль/л.
ПР(CaHPO4) =2,7*10-7. Выберите верные утверждения:
ПР (AgCl)=1,8*10-10 Кнест. диамминсеребра (1)=10-8
Выберите верные утверждения, характеризующие равновесие в аммиачном растворе хлорида серебра:
Установите соответствие между растворами и их характеристиками
раствор - характеристика
|
ненасыщенный
|
в нем осадок растворяется
|
насыщенный
|
концентрация ионов постоянна
|
перенасыщенный
|
ПР меньше ПИ
|
Выберите вещество, добавление которого приведет к увеличению растворимости сульфата кальция в воде:
Установите соответствие между растворами и их характеристиками
|
ненасыщенный
|
ПР больше ПИ
|
насыщенный
|
содержит максимально возможное при данных условиях количество растворенного вещества
|
перенасыщенный
|
скорость растворения меньше скорости осаждения
|
Возможно ли полное растворение 0,1 г хлорида серебра в 1л воды при стандартных условиях?
ПР (AgCl) = 1.8*10-10
Вычислить равновесную концентрацию ионов бария в насыщенном растворе хромата бария.
ПР (ВаСrО4)=1,1*10-10.
В 1л насыщенного раствора сульфата кальция при температуре 20 С содержится 2,04 г вещества. Рассчитайте произведение растворимости.
Рассчитать равновесную концентрацию ионов серебра в насыщенном растворе AgI. ПР = 2.3*10-16
Установите соответствие между терминами в левом столбце и утверждениями в правом.
|
химическое строение
|
Изображается структурной формулой
|
конфигурация
|
Определяется типом гибридизации
|
конформация
|
Изменяется при повороте молекулы вокруг сигма-связи
|
Установить соответствие между утверждением в левом столбце и видом изомерии.
|
Смесь изомеров невозможно разделить
|
конформационная изомерия
|
Изомеры отличаются расположением заместителей вокруг асимметрического атома углерода
|
оптическая изомерия
|
Разновидность структурной изомерии
|
изомерия углеродного скелета
|
К какому электроду при электрофорезе будет передвигаться белок каталаза крови (pI 7) в растворе аммиака, наполовину нейтрализованного соляной кислотой? рКаммиака=4,75
|
К аноду
|
рН = 9.25
|
К какому электроду при электрофорезе будет передвигаться белок химотрипсин сока поджелудочной железы с (pI 8,6) в сантимолярном растворе аммиака. Кдисс(NН3)=1,8*10-5.
|
К аноду
|
рН = 10.625
|
Альбумин куриного яйца имеет значение изоэлектрической точки 4,8. К какому электроду при электрофорезе будет передвигаться белок в растворе уксусной кислоты, наполовину нейтрализованной щелочью? рК СН3СООН = 4,8.
|
Белок неподвижен
|
рН = 4.8
|
В каком растворе можно электрофоретически разделить аминокислоты глицин рI 6,1 и глутаминовую кислоту pI 3,09:
|
0,01М растворе уксусной кислоты рК=4,75
|
рН = 3.375
|
Установите соответствие между аминокислотой и ее названием и характером среды водного раствора
Аминокислота Реакция среды
|
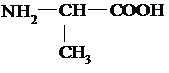
|
Аланин, среда слабокислая, близкая к нейтральной
|

|
Аспарагиновая кислота, среда кислая
|

|
Глутамин, среда слабокислая, близкая к нейтральной
|

|
Аргинин, среда щелочная
|
Установите соответствие между названием аминокислоты и ее формулой, и характером среды водного раствора
Аминокислота -------------------- Формула, среда водного раствора
|
Тирозин
|
 среда нейтральная
среда нейтральная
|
Пролин
|
 среда нейтральная
среда нейтральная
|
Фенилаланин
|
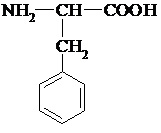 среда нейтральная
среда нейтральная
|
Глутамин
|
 среда нейтральная
среда нейтральная
|
Выберите дипептиды, растворы которых имеют щелочную среду
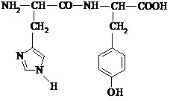 Выберите формулу, отвечающую форме гистидина в растворе при рН<<pI
Выберите формулу, отвечающую форме гистидина в растворе при рН<<pI
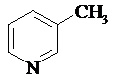
Установите соответствие между схемой процесса и преимущественным продуктом
Процесс ----------------------- Преимущественный продукт
|
Пиридин + хлорметан
|
|
Пиррол +хлорметан
|

|
Пиримидин + хлорметан
|

|
Фенол + хлорметан
|

|
Выберите верные утверждения, относящиеся к понятию "ароматичность"
Ароматическими являются только циклические соединения
К ароматическим соединениям относятся все перечисленные вещества: нафталин, пиримидин, пурин
Ароматические соединения вступают в реакции электрофильного замещения, реакции присоединения нехарактерны, протекают в жестких условиях
Выберите верные утверждения
Выберите растворы, буферная емкость которых по кислоте равна буферной емкости по щелочи
бикарбонатный буферный раствор, полученный сливанием равных объемов эквимолярных растворов гидрокарбоната натрия и угольной кислоты
ацетатный буферный раствор, полученный нейтрализацией уксусной кислоты гидроксидом натрия на 50%
Выберите растворы, которые стойко поддерживают рН=5 аммонийный буферный раствор, содержащий по 0,05 моль эквивалента аммиака и хлорида аммония К ионизации аммиака = 1,75*10-5.
ацетатный буферный раствор, содержащий по 0,01 моль эквивалента ацетата натрия и уксусной кислоты К диссоциации уксусной кислоты = 1,75*10-5
ацетатный буферный раствор, содержащий 0,05 моль эквивалента ацетата натрия и 0,05 моль эквивалента уксусной кислоты Кдисссоциации уксусной кислоты = 1,75*10-5
Выберите пары растворов с одинаковой массовой долей (плотность растворов принять 1 г/мл; расчеты с точностью до тысячных)
0,01 молярный раствор глюкозы и 0,01 молярный раствор фруктозы
раствор, содержащий 0,141 моль сульфата натрия и раствор, содержащий 0,122 моль фосфата натрия в каждом литре раствора
0,01 М раствор пропановой кислоты и 0,01 М раствор этилформиата
Выберите пары растворов с одинаковой молярной концентрацией (плотность растворов принять 1 г/мл)
раствор, содержащий 1,80 г глюкозы и раствор, содержащий 3,42 г сахарозы в каждом литре раствора
раствор, содержащий 36,5 г соляной кислоты и раствор, содержащий 40,0 г гидроксида натрия в 1 литре раствора
20% раствор глюкозы и 20% раствор фруктозы
сантимоляльный раствор бутановой кислоты и сантимоляльный раствор 2-метилпропановой кислоты
Установите соответствие между реагентом, добавленным в буферный раствор, и уравнением реакции, протекающей в растворе
|
Бикарбонатный буферный раствор + соляная кислота
|
|
Бикарбонатный буферный раствор + гидроксид натрия
|
|
Фосфатный буферный раствор + соляная кислота
|
|
Фосфатный буферный раствор + гидроксид натрия
|
|
Выберите верные утверждения
При добавлении в любой буферный раствор сильной кислоты рН незначительно уменьшается
При небольшом разбавлении буферного раствора водой рН не изменяется
При добавлении в буферный раствор сильной кислоты число моль эквивалента сопряженного основания убывает, сопряженной кислоты возрастает
Выберите верные утверждения
бикарбонатная буферная система в крови действует кооперативно с гемоглобиновой и оксигемоглобиновой буферными системами
рН бикарбонатной буферной системы зависит от парциального давления углекислого газа воздуха, находящегося в равновесии с кровью
один из процессов восполнения щелочного резерва крови может быть описан уравнением
Выберите верные утверждения:
При добавлении к фосфатному буферному раствору гидроксида бария
рН раствора незначительно увеличивается
концентрация дигидрофосфата-аниона убывает, гидрофосфата-аниона - возрастает
Расположите процессы в ряд по возрастанию изобарно-изотермического потенциала (Ео (О2/Н2О)=0,82 В.):
|
Цитохром с1 + О2 Еоцитохром с1=0,22 В
|
Цитохром с + О2 Еоцитохром с =0,26 В
|
Цитохром а + О2 Еоцитохром а =0,29 В
|
Выберите правильное утверждение для ОВР с учетом направления самопроизвольной реакции:
С2Н5ОН + НАД+ ; СН3СОН + НАДН + Н+
Eo’(ацетальдегид/этанол)= -0,20 В; Eo’ (НАД+/НАДН)= -0,320 В
Выберите одну пару утверждений, которые правильно характеризуют самопроизвольную ОВР:
С2Н5ОН + НАД+ ; СН3СОН + НАДН + Н+
Eo’(ацетальдегид/этанол)= -0,20 В; Eo’ (НАД+/НАДН)= -0,320 В
|
ацетальдегид - окислитель
|
НАДН отдает 2 протона и 2 электрона
|
Выберите правильное утверждение для ОВР с учетом направления самопроизвольной реакции: 2MnO4- + 5NO2- + 6H+ ; 2Mn2+ + 5NO3- + 3H2O
Eo (MnO4 / Mn2+)=1,51B; Eo (NO3 /NO2 )=0,94B
Выберите одну пару утверждений, которые правильно характеризуют самопроизвольную ОВР: 2MnO4 + 5NO2 + 6H+ ; 2Mn2+ + 5NO3 + 3H2O
Eo (MnO4 / Mn2+)=1,51B; Eo (NO3 /NO2 )=0,94B
Стандартный окислительно-восстановительный потенциал системы пируват/лактат при рН=7 составляет - 0,180 В. Выберите верные утверждения:
Выберите из списка растворы, буферная емкость которых по щелочи меньше буферной емкости по кислоте
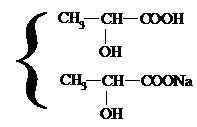
Установите соответствие между смешиваемыми растворами и составом конечного раствора
|
Эквимолярные растворы молочной кислоты-100 мл и гидроксида натрия-100 мл
|

|
200 мл 0,01 М раствора молочной кислоты и 100 мл 0,01М раствора гидроксида натрия
|
|
200 мл 0,01 М раствора гидроксида натрия и 0,01 моль углекислого газа
|

|
200 мл 0,01 М раствора гидроксида натрия и 0,001 моль углекислого газа
|
NaHCO3
|
Выберите из списка буферные растворы, которые противодействуют изменению рН в организме человека
Установите соответствие между способом выражения концентрации и формулой
|
Молярная концентрация
|
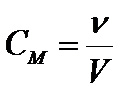
|
Молярная концентрация эквивалента
|

|
Моляльная концентрация
|

|
Массовая доля вещества
|

|

Выберите формулу, отвечающую форме гистидина в растворе при рН<<pI

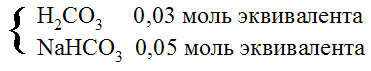

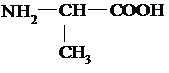



 среда нейтральная
среда нейтральная среда нейтральная
среда нейтральная среда нейтральная
среда нейтральная







