
5 курс / Сексология (доп.) / Подготовка_и_ведение_супружеских_пар_при_использовании_вспомогательных
.pdfУ женщин, включенных в программу ВРТ, отмечается снижение активности процессов фолликулогенеза и оогенеза при проведении гонадотропной стимуляции, более худшее качество ооцитов, заключающееся в снижении показателей их оплодотворяемости, последующего дробления развившихся эмбрионов, и более низкую частоту имплантации при различных формах наружного генитального эндометриоза, и особенно при сочетании с аденомиозом.
С целью повышения вероятности наступлении беременности в программе ЭКО и ПЭ рекомендуется предварительное двухэтапное комбинированное лечение эндометриоза, включающее оперативное лечение с коагуляцией эндометриоидных очагов и последующее медикаментозное лечение, направленное на угнетение гонадотропной функции гипофиза путем введения депо формы аГнРГ в течение 3-6 месяцев после оперативного вмешательства. Использование аГнРГ в послеоперационном периоде способствует смягчению проявления симптомов данного заболевания, включая болевой синдром, уменьшению размера, количества эндометроидных поражений, препятствует образованию новых эндометриоидных очагов, нормализует анатомо-физиологические и рецепторные особенности эндометрия и баланс локального иммунитета, функцию клеточного звена и гомеостаза перитонеальной полости, что улучшает результаты в отношении качества, количества ооцитов и имплантации эмбрионов, повышает вероятность наступления беременности в программе ЭКО.
При увеличении промежутка между комбинированным лечением эндометриоза и временем включения в программу ЭКО и ПЭ наблюдается снижение частоты оплодотворяемости ооцитов, так как начинают прогрессировать оставшиеся очаги эндометриоза, либо появляются новые гетеротопии, что способствует повышению базального уровня ЛГ, преждевременному выбросу эндогенного ЛГ и формированию аномальных яйцеклеток в программе ВРТ.
Следует рекомендовать лечение бесплодия методом ЭКО и ПЭ супружеским парам при отсутствии беременности в течение 1 года после завершенного комбинированного лечения. При III – IV стадии наружного генитального эндометриоза, при сочетании с аденомиозом, в возрасте женщины старше 35 лет, резекции яичников в анамнезе, сочетании нескольких факторов бесплодия рекомендуется использовать методы ВРТ непосредственно после окончания комбинированного лечения эндометриоза.
— 21 —
ПРИМЕНЕНИЕ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВ И ЭНДОСКОПИИ В ПОДГОТОВКЕ ПАЦИЕНТОК К ПРОГРАММЕ ЭКО
Необходимость тщательной коррекции патологических состояний, требующих оперативных вмешательств, на этапе подготовки пациенток к программе ЭКО диктуется влиянием данной патологии на состояние здоровья пациентки, эффективность проводимой процедуры и имплантации эмбрионов.
Среди пациенток, участвующих в программе ЭКО и ПЭ, значительную часть составляют женщины с патологическими изменениями в маточных трубах. Следует отметить, что наличие в анамнезе повторных реконструктивно-пластических операции на маточных трубах, является фактором риска возникновения внематочной беременности, в том числе и после проведения программы ЭКО и ПЭ. Учитывая, что при гидросальпинксе реконструктивно-пластические операции неэффективны, а содержимое гидросальпинкса оказывает токсическое влияние на эмбрионы, наличие сактосальпинкса является противопоказанием к проведению программы ЭКО и ПЭ и в качестве подготовки к использованию методов ВРТ показана тубэктомия путем лапароскопического доступа.
При наличии доброкачественных опухолей яичника отмечается неадекватная реакция яичников на гонадотропную стимуляцию, а также повышается онкологическая настороженность в отношении данной пациентки. Удалять кисты яичников предпочтительно путем цистэктомии без резекции ткани яичника, что позволяет максимально сохранить фолликулярный аппарат. Оперативные вмешательства на яичниках следует выполнять максимально бережно, с пониманием того, что исходом любой хирургической травмы является уменьшение овариального резерва.
Наибольшее нарушение фолликулогенеза возникают при использовании дополнительной коагуляции. В связи с чем при ретенционных образованиях предпочтение должно быть отдано гормональным и щадящим методам лечения, при доброкачественных образованиях – методике их энуклеации
В процессе предоперационной подготовки таким пациенткам следует провести определение в сыворотке крови опухолевого маркера СА-125, обследование желудочно-кишечного тракта.
При развитии внематочной беременности после применения ВРТ несмотря на наличие современных технических возможностей лапароскопии в выполнении оперативных вмешательств на трубах рекомендуется выполнить тубэктомию с тщательным иссечением всего истмического отдела трубы для профилактики имплантации эмбриона в культе маточной трубы
— 22 —
при проведении последующих попыток ЭКО и ПЭ.
С целью повышения эффективности использования ВРТ на втором этапе – ПЭ используется оценка состояния шейки матки, цервикального канала и эндометрия с помощью эндоскопических методов диагностики.
Проведение расширенной кольпоскопии целесообразно всем пациенткам, планирующим программу ЭКО и ПЭ, в связи с наличием у них длительно текущих воспалительных процессов всех отделов половых органов, одним из проявлений которых является эндоцервицит. Обязательным обследованием перед использованием ВРТ является онкоцитологическое исследование мазков из цервикального канала, биопсия участка шейки матки с последующим гистологическим исследованием при наличии подозрительного очага при проведении расширенной кольпоскопии Выявление любых фоновых и предраковых заболеваний шейки матки требует предварительного лечения шейки матки с последующей контрольной расширенной кольпоскопией и контролем излеченности перед включением в программу ЭКО и ПЭ.
Использование диагностической гистероскопии показано всем пациенткам, включенным в программу ЭКО и ПЭ, после нескольких неудачных попыток, а также при наличии патологии эндометрия, в частности при визуализации гиперплазии или полипа эндометрия по данным УЗИ на 5 – 7 день менструального цикла, при подозрении на наличие синехий полости матки, внутриматочной перегородки. При гистероскопическом подтверждении гиперплазии или полипа эндометрия необходимо удаление последнего с гистологическим исследованием и последующей гормональной терапии не менее 3 месяцев для подготовки эндометрия к ПЭ.
При гистероскопическом подтверждении внутриматочных синехий проводится рассечение рубцово-спаечных изменений легкой степени и диссекция спаек микроножницами или электродом гистерорезектоскопа при выраженных внутриматочных сращениях. В послеоперационном периоде рекомендуется использование внутриматочных контрацептивов и назначение эстроген-гестагенных препаратов на 3 месяца. При наличии выраженных внутриматочных синехий рекомендуется проведение контрольной диагностической гистероскопии через 3 месяца. При отсутствии эффекта от проводимой терапии супружеской паре предлагается воспользоваться программой суррогатного материнства.
Диагностическая гистероскопия также используется с целью верификации аденомиоза и последующей подготовкой пациентки к программе ВРТ с использованием аГнРГ, в связи с тем, что у данного контингента больных отмечается более низкая частота имплантации
— 23 —
С целью повышения вероятности наступлении беременности в программе ЭКО и ПЭ женщинам при подозрении на аденомиоз рекомендуется гистероскопическая верификация данного заболевания и последующее медикаментозное лечение, направленное на угнетение гонадотропной функции гипофиза путем введения депо формы аГнРГ в течение 3-6 месяцев после оперативного вмешательства. Использование аГнРГ в послеоперационном периоде способствует смягчению проявления симптомов данного заболевания, включая болевой синдром, нормализует анатомо-физиологические и рецепторные особенности эндометрия и баланс локального иммунитета, функцию клеточного звена и гомеостаза перитонеальной полости, что улучшает результаты в отношении имплантации эмбрионов.
При неудачных попытках ЭКО с диагностической целью проводится на 8-10 день менструального цикла гистероскопия с гистологическим исследованием биоптатов эндометрия с целью верификации хронического эндометрита, как фактора снижающего эффективность программы ВРТ. Значительная вариабельность данных о распространенности хронического эндометрита, трудности верификации диагноза, необходимость проводить инвазивные методы исследования, отсутствие четких критериев излеченности создают особые сложности в диагностике данного патологического процесса и приводят к недооценке роли данного заболевания в нарушении репродуктивной функции. Повреждение ткани при хроническом воспалительном процессе вызывает формирование многоуровневого каскада патологических реакций, нарушение нормальной циклической трансформации, активацией цитокинов, факторов роста, протеолитических ферментов, что индуцирует изменение ангиоархитектоники ткани, склерозированию и нарушению рецептивности ткани и соответственно ухудшает условия для имплантации эмбриона.
Комплексная терапия хронического эндометрита основываться на выявлении этиологического фактора (антибиотикотерапия) и должна включать физиотерапию (ультразвук на низ живота, магнитотерапия, ультрафиолетовое облучение крови) и метаболическую терапию (актовегин по 1 таблетке 2 раза в день 4 недели, вобензим по 3 драже 3 раза в день 30 дней) на фоне приема комбинированных оральных контрацептивов под контролем коагулограммы и Д-димеров.
Условием для проведения ИСМ и ИОСД, как модификации ВРТ, является наличие хотя бы одной свободно проходимой функционально полноценной маточной трубы у пациентки. Визуализация внутриматочной патологии, патологии маточных труб, спаечного процесса возможна при
— 24 —
выполнении рентгеновской гистеросальпингографии с использованием контрастных сред, мультиспиральной компьютерной томографии (МСКТ), гидросонографии как в двухмерном режиме, так и в режиме объемной трехмерной реконструкции. МСКТ позволяет точно определить характер патологического процесса, его локализацию, взаимосвязь с соседними органами, а также уточнить анатомическое и топографическое состояние органов малого таза, оценить анатомическую проходимость маточных труб, их топографоанатомические особенности отхождения и расположения, взаимоотношение с соседними органами, состояние эндометрия.
В заключение следует отметить, что среди факторов, определяющих успех реализации программы ЭКО, является овариальный резерв, на который оказывают влияние, прежде всего возраст и хирургическая травма фолликулярного аппарата, а также состояние эндометрия как фактора определяющего успешную имплантацию. Следовательно, с возрастом и в результате оперативных вмешательств на яичниках уменьшается количество фолликулов, ооцитов, эмбрионов, что резко снижает эффективность программы ВРТ и наступления желанной беременности. Очевидно, что сложившаяся тактика длительного обследования, лечение повторными курсами бесплодной супружеской пары, а также необоснованных хирургических вмешательств на яичниках требует пересмотра.
МУЖСКОЙ ФАКТОР БЕСПЛОДИЯ В ПРОГРАММЕ ВРТ
За последние годы нарушение репродуктивной функции мужчин, состоящих в бесплодном браке, приобрело особую значимость, так как отмечается увеличение частоты инфертильного состояния мужчин, достигающей 30-50%. Это связано с увеличением инфекционновоспалительных заболеваний мочеполовой системы, аномалий развития половых органов, влиянием вредных факторов окружающей среды, аллергизацией и другими факторами.
Среди всех методов оценки фертильности мужчины основным является оценка спермограммы. Относительная стабильность показателей спермограммы в течение определенного времени позволяет ограничиться одним анализом спермы при нормозооспермии, получаемом при воздержании не менее 3 и не более 7 дней. При патозооспермии анализ выполняется дважды с промежутком 14 дней. Если результаты анализа резко отличаются друг от друга, то выполняют третий анализ. Из двух спермограмм принимается во внимание лучший результат. Самым высоким информативным показателем нарушения фертильности спермы является
— 25 —
нарушение морфологии и подвижности сперматозоидов. В настоящее время приняты следующие нормативные показатели для оценки спермограммы, рекомендованные ВОЗ (таблица 1)
|
|
|
|
|
|
Таблица 1 |
|
|
Нормативные показатели фертильной спермы |
||||
|
Показатели спермограммы |
Качество спермы |
||||
|
|
Объем |
|
≥2,0 мл |
||
|
|
рН |
|
7,2 – 7,8 |
||
|
Вид и вязкость |
нормальный, < 1 см |
||||
|
|
Разжижение |
<60 минут |
|||
|
Концентрация |
≥20,0х106/мл |
||||
|
Подвижность |
≥25% категории «а» |
||||
|
категория |
«а» |
|
быстрое |
≥50% категории «а +b» |
|
линейное прогрессивное движение |
|
|||||
|
категория |
«b» |
медленное |
|
||
|
|
|
|
|
|
|
линейное |
и |
нелинейное |
|
|||
прогрессивное движение |
|
|
||||
|
Морфология |
≥30% нормальных форм |
||||
|
|
|
|
|
|
(≥14% по строгим критериям |
|
|
|
|
|
|
Крюгера) |
|
Жизнеспособность |
≥50% живых сперматозоидов |
||||
|
Агглютинация |
отсутствует |
||||
|
|
МАР-тест |
<50% подвижных |
|||
|
|
|
|
|
|
сперматозоидов, покрытых |
|
|
|
|
|
|
антителами |
|
|
Лейкоциты |
<1,0х106/мл |
|||
|
|
Флора |
|
отсутствует или <103КОЕ/мл |
||
Нормозооспермия – нормальные показатели спермограммы. Олигозооспермия – концентрация сперматозоидов <20,0х106/мл. Тератозооспремия – морфологически нормальных форм
сперматозоидов 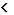 30% (<14% по строгим критериям Крюгера) при нормальных показателях количества и подвижных форм.
30% (<14% по строгим критериям Крюгера) при нормальных показателях количества и подвижных форм.
Астенозооспермия – подвижность сперматозоидов категории «а» <25% или категории «а+b»<50%, при нормальных показателях количества и морфологии форм.
Олигоастенотератозооспермия – сочетание трех вариантов патоспермии.
— 26 —
Азооспермия – отсутствие сперматозоидов в эякуляте. Аспермия – остутствие эякулята.
Следует отметить, что анализ морфологических характеристик наиболее важен, так как сперма с большим количеством патологических форм сперматозоидов, даже при отличных других показателях, нефертильна. Наступающая при этом беременность заканчивается выкидышом в ранние сроки или наступлением внематочной беременности.
Обследование и лечение мужчин с субфертильной и нефертильной спермой осуществляется урологом-андрологом. Проводится инфекционный скрининг, гормональное, иммунологическое и медико – генетическое обследование. Также проводится УЗИ органов мошонки, а при азооспермии пункционная биопсия или аспирационная биопсия яичка или придатка.
В лечении мужского бесплодия, когда консервативные и хирургические методы безуспешны, применяют программу ЭКО, а также следующие модификации ВРТ: ИОСМ, ИОСД, ЭКО+ИКСИ.
Технология ИКСИ обеспечивает оплодотворение in vitro при тяжелых формах олигоастенотератозооспермии. При азооспермии, обусловленной обструкцией семявыводящих путей, необходимые для инъекции в яйцеклетку сперматозоиды могут быть получены с помощью пункции яичка или придатка яичка.
ОСНОВНЫЕ ПРИНЦИПЫ РЕАЛИЗАЦИИ ПРОГРАММЫ ЭКО
Этапы программы ЭКО:
1.отбор и обследование пациентов;
2.КИСО;
3.пункция фолликулов (хирургический забор яйцеклеток);
4.инсеминация ооцитов или проведение ИКСИ и культивирование эмбрионов, при наличии показаний выполнение предимплантационой диагностики;
5.ПЭ в полость матки;
6.поддержка лютеиновой фазы после ПЭ в полость матки;
7.диагностика беременности ранних сроков.
Проведение ЭКО возможно с использованием индукции
суперовуляции или в естественном менструальном цикле.
Для индукции суперовуляции могут применяться только препараты, разрешенные для использования на территории Республики Беларусь. Выбор протокола индукции суперовуляции осуществляется лечащим врачом индивидуально. Коррекция доз вводимых препаратов и внесение изменений в
— 27 —
протокол индукции суперовуляции осуществляется на основании данных ультразвукового мониторинга за ростом фолликулов и эндометрия. Для индукции суперовуляции используются гонадотропины (человеческий менопаузальный гонадотропин — чМГ(менопур, хумог), рФСГ (гонал-Ф, пурегон), ХГ (прегнил, овитрель); аГнРГ (диферелин, бусерелин, декапептил), антагонисты гонадотропин-рилизинг-гормона – антГнРГ (цетротид, оргалутран)
КИСО требует тщательного ультразвукового мониторинга за процессами, происходящими в яичниках и матке. Мониторинг позволяет определить момент начала гонадотропной стимуляции, оценить ответ яичников и состояние эндометрия, контролировать эффективность стимуляции яичников и корректировать режим и дозы применяемых препаратов, прогнозировать возможность развития СГЯ, диагностировать преждевременную овуляцию. Важнейшей задачей мониторинга является определение момента для назначения ХГ, т.е. завершения гонадотропной стимуляции.
Ультразвуковой мониторинг начинается со 2-го дня менструального цикла. Следующее УЗИ проводится на 5-й день, а с 7-го дня исследования выполняются через день. При достижении фолликулами диаметра 15 мм УЗИ проводится ежедневно вплоть до назначения овуляторной дозы ХГ.
Критерии завершения КИСО и назначения ХГ являются толщина эндометрия (8 мм и более) и многослойная его структура, адекватный кровоток в сосудах матки, а также наличие в когорте не менее 50% крупных фолликулов (диаметром 18 мм и более).
Для завершения созревания ооцитов вводится ХГ в дозе 5000-10000 ME однократно).
Пункция фолликулов и аспирация ооцитов производится через 34-36 часов от момента введения ХГ. Процедура выполняется амбулаторно, в асептических условиях, под внутривенной анестезией. Пункция фолликулов обычно осуществляется трансвагинально под ультразвуковым контролем с помощью специальных пункционных игл. После оперативного вмешательства пациентка должна находиться под наблюдением врача не менее 2-х часов.
Фолликулярную жидкость, полученную в результате пункции фолликулов, помещают в чашку Петри. Аспират исследуют под стереомикроскопом с 10-50-кратным увеличением. При этом проводится оценка качества полученных ооцитов, после чего их переносят в среду для культивирования. Чашку с ооцитами помещают в инкубатор с температурой
— 28 —
37°С и 5% концентрацией С02 в газовой среде. Обычно ооциты оставляют в инкубаторе на 4-6 часов до инсеминации.
Как нативная, так и криоконсервированная сперма перед использованием должна быть обработана для того, чтобы отмыть сперматозоиды от плазмы и выделить фракцию морфологически нормальных и высокоподвижных сперматозоидов методом центрифугирования — флотации и градиентного центрифугирования.
При тяжелых формах олиоастенотератозооспермии проводят манипуляцию ИКСИ, которая включает в себя обездвиживание сперматозоида, нарушение целостности мембраны ооцита, введение сперматозоида в цитоплазму ооцита.
Контроль оплодотворения обычно проводится через 12-18 часов, когда пронуклеусы четко визуализируются. Зиготы переносят в свежую культуральную среду, где происходит начальное развитие эмбрионов. Перенос эмбрионов в полость матки может быть осуществлен на разных стадиях, начиная со стадии зиготы и заканчивая стадией бластоцисты (на 2 – 5-е сутки развития).
В полость матки переносят не более 2-3-х эмбрионов. Перенос рекомендуется проводить после предварительного ультразвукового исследования, во время которого измеряется длина цервикального канала и полости матки, толщина эндометрия и оценивается состояние яичников. Для переноса эмбрионов используются специальные катетеры, которые вводятся в полость матки через цервикальный канал.
Поддержка лютеиновой фазы стимулированного менструального цикла обычно начинается со дня пункции фолликулов и проводится прогестероном (внутримышечно, 25 мг в день), утрожестаном (интравагинально, 300-600 мг), дюфастоном (30-40 мг/сутки), крайноном (1 аппликатор в день) до дня обследования на β-ХГ в крови у женщины.
При отсутствии риска СГЯ и у женщин старше 39 лет поддержка лютеиновой фазы цикла может включать также введение препаратов ХГ в дозах 500-3000 ЕД, которые назначаются в день ПЭ, а затем дважды с интервалом в 2-3 дня.
Диагностика беременности по содержанию β -ХГ в крови через 12-14 дней от момента ПЭ. Ультразвуковая диагностика беременности может проводиться с 21 дня после ПЭ. Диагноз беременности оправдан только при визуализации плодного яйца во время эхографического исследования.
Возможные осложнения при использовании программы ЭКО и ПЭ:
1.СГЯ
2.аллергические реакции на препараты для индукции суперовуляции и
—29 —
поддержки лютеиновой фазы стимулированного менструального цикла;
3.наружное и внутреннее кровотечение;
4.острое или обострение хронического воспаления органов малого таза
5.неразвивающаяся беременность
6.многоплодная маточная беременность
7.гетеротопическая беременность
СУРРОГАТНОЕ МАТЕРИНСТВО
При наличии у пациентки противопоказаний к вынашиванию беременности одним из путей преодоления бесплодия является использование программы «Суррогатное материнство»
Суррогатная мать – это женщина, у которой беременность наступила после переноса эмбриона, полученного в результате оплодотворения ооцитов третьей стороны спермой третьей стороны. Супружеская пара, которым принадлежит эмбрион, и «суррогатная» мать дают информированное согласие па участие в программе и заключают договор с медицинским центром ВРТ о проведении медицинской услуги.
Суррогатными матерями могут быть родственницы и знакомые супружеской пары, а также женщины, добровольно согласившиеся на участие в данной программе в возрасте от 20 до 35 лет, имеющие собственного здорового ребенка при отсутствии медицинских противопоказаний к реализации программы ВРТ.
Медицинское обследование суррогатной матери, генетической матери и их супругов проводится врачами-терапевтами в организациях здравоохранения только при наличии нотариально удостоверенного договора суррогатного материнства.
Медицинские показания для генетической матери к суррогатному материнству:
1.отсутствие матки (врожденное или приобретенное)
2.деформация полости или шейки матки при врожденных пороках развития или в результате заболеваний
3.синехии полости матки, неподдающиеся терапии
4.соматические заболевания, при которых вынашивание беременности противопоказано
5.неудачные попытки ЭКО при неоднократном получении эмбрионов высокого качества, перенос которых не приводил к наступлению беременности
—30 —
