
книги / Плавка цветных металлов
..pdfТехнологический процесс плавки титановых сплавов в любой ПЗУ проводится в следующей последовательности: подготовка печи к плавке, установка и приварка расходуемого электрода к огарку или электрододержателю, создание вакуума в камере печи, плавка металла и заливка форм.
Приварка расходуемого электрода производится в вакууме
состаточным давлением 67–13 Па. Электрододержатель (огарок) подводится к электроду, и за счет электрической дуги на торце электрода расплавляется лунка жидкого металла. Далее выключается электрический ток и электрододержатель прижимается к оплавленному электроду.
Герметизация печи и откачка вакуума длятся от 20 до 40 мин. Пока в ПЗУ наибольшее применение нашли графитовые тигли
сводяным охлаждением стенок через водоохлаждаемый медный токоподвод. Дно охлаждается за счет теплового излучения. Толщина стенок тигля – от 60 мм в нижней части до 20 мм вверху. Толщина дна достигает значений 100 мм. Тигли могут быть изготовлены из меди или нержавеющей стали, но их применение сдерживается из-за опасности проплавления и взрыва.
Перспективным методом является индукционный способ плавки в «холодных» тиглях.
Вопросы для самоконтроля
1.Почему необходима вакуумная плавка титана?
2.Какая глубина вакуума необходима при плавке титана?
3.Как влияют на свойства титановых сплавов примеси?
4.Принцип работы вакуумной гарнисажной печи.
5.Что такое гарнисаж?
6.Из чего выполнен тигель гарнисажной печи?
7.Какова оптимальная толщина гарнисажа?
8.Какая сила тока необходима для плавления титана?
9.Можно ли переплавлять отходы в гарнисажных печах?
10.Как готовят отходы к переплавке?
111
11.Можно ли вести разливку расплава с включенной дугой?
12.Где размещается литейная форма при гарнисажной плавке?
13.Из чего выполняются расходуемые электроды?
14.Как осуществляется приварка электродов?
15.В какие литейные формы заливают титановые сплавы?
16.Что предусмотрено в ПЗУ для улучшения заполняемости
форм?
17.Назовите основной недостаток печей периодического дей-
ствия.
112
6.ПЛАВКА МЕДИ И МЕДНЫХ СПЛАВОВ
Впромышленности широко используется как чистая медь, так
иразличные литейные и деформируемые сплавы на медной основе: оловянные бронзы, безоловянные (специальные) бронзы и латуни.
Оловянные литейные бронзы (ГОСТ 613–79) обладают хорошими литейными, механическими и эксплуатационными (коррозионными и антифрикционными) свойствами. Из них изготовляют арматуру, подшипники, шестерни, втулки, работающие в условиях трения. Оловянные бронзы имеют большой интервал кристаллизации (150–200 °С), поэтому отливки могут быть подвержены газоусадочной пористости. Наиболее вредными примесями являются алюминий и кремний.
Безоловянные бронзы (ГОСТ 493–79) по механическим, коррозионным и антифрикционным свойствам не уступают оловянным, а по некоторым превосходят их. Более широкое распространение получили алюминиевые бронзы. Из них изготовляют детали зубчатых и червячных передач, гребные винты и другие детали. Алюминиевые бронзы относятся к сплавам с узким интервалом кристаллизации.
Литейные латуни (ГОСТ 17711–93) в зависимости от состава
имеют широкий диапазон механических и эксплуатационных свойств. Для изготовления фасонных отливок чаще всего используют кремнистую латунь ЛЦ16К4 и свинцовистую латунь ЛЦ40С, а также высокопрочные сложнолегированные латуни
(ЛЦ23А6Ж3Мц2 и др.).
В чистом виде медь применяют для изготовления таких фасонных отливок, как фурмы доменных печей и кислородных конвертеров, а также токопроводящих фасонных изделий [6].
Плавка чистой меди и каждой группы сплавов на ее основе имеет свои отличия, но они базируются на общих закономерностях, которые рассмотрены ниже.
113

6.1.Физико-химические особенности плавки меди
имедных сплавов
Наиболее важными для плавки меди являются такие физикохимические процессы, как взаимодействие расплава с кислородом, водородом, серой, атакже сфутеровкой печи, шлаками и флюсами[17].
Плавку меди можно вести на воздухе, в среде защитных газов, под защитным покровом и в вакууме. При плавке на воздухе медь окисляется до закиси Сu2О, которая в дальнейшем растворяется в расплаве. При 1200 °С в меди может быть растворено до 1,5 % кислорода в виде Сu2О. При кристаллизации закись меди образует эвтектику Сu–Сu2О, которая располагается по границам зерен и снижает пластичность сплавов.
Расплавленная медь взаимодействует с сернистым газом, образуя растворимый сульфид Сu2S, который также ухудшает пластические свойства.
Медь в ходе плавки интенсивно поглощает водород. При значениях температуры перегрева до 1100–1300 °С растворимость водорода может достигать 5–7 см3/100 г. Источником водорода при плавке меди и медных сплавов служит водяной пар, а также влага, попадающая в расплав из свежей футеровки, шихты и флюсов. Наибольший вклад в насыщение водородом вносит водяной пар. Его парциальное давление в печной атмосфере в реальных условиях колеблется в пределах от 0,0001 до 0,02 МПа. В практических расчетах допустимо считать, что РН2 ≈ РН2 О, и для расчета равновесной кон-
центрации водорода в расплаве пользоваться известным уравнением Сивертса
[Н] = KН РН2 ,
где KН – растворимость водорода в сплаве при расчетной температуре и давлении РН2 = 0,101 МПа [12].
Растворение водорода идет тем интенсивнее, чем выше температура (рис. 30). При температуре плавления растворимость возрастает скачкообразно в 2–3 раза. По сравнению с другими металлами
114
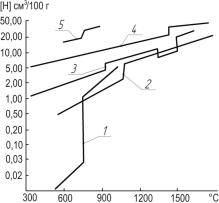
растворимость водорода в меди не так уж и велика, но существенная разность значений растворимости в жидком и твердом состояниях указывает на возможность появления газовой пористости.
Рис. 30. Влияние температуры на растворимость водорода в различных металлах: 1 – в алюминии; 2 – в меди;
3 – в железе; 4 – в никеле; 5 – в магнии
Легирующие элементы и примеси меняют растворимость водорода. Так, между содержанием кислорода и водорода, как видно из рис. 31, в расплаве меди устанавливается динамическое равновесие. Чем больше в меди кислорода, тем меньше будет ее насыщение водородом, и наоборот. Влияние других элементов показано на рис. 32. Более склонны к насыщению водородом бронзы и латуни, легированные никелем, железом, хромом и марганцем.
При кристаллизации и охлаждении отливок избыточный водород ухудшает свойства медных сплавов, способствует образованию в отливках газовой или газоусадочной пористости. Предельно допустимая концентрация водорода зависит от скорости охлаждения. При литье в кокиль (быстрое охлаждение) можно допустить более высокое содержание водорода, чем при литье в песчаные формы.
В любом случае при плавке необходимо принимать меры против насыщения расплава водородом и проводить дегазацию перед разливкой.
115
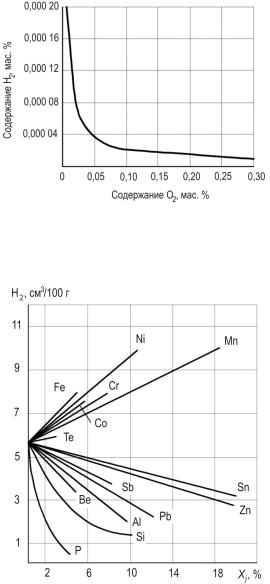
Рис. 31. Зависимость растворимости водорода в меди от содержания кислорода при 1473 К (кривая Аллена)
Рис. 32. Влияние некоторых элементов (Хi) на равновесную растворимость водорода в меди при 1423 К и РН2 = 0,101 МПа
116
Расплавы меди и медных сплавов могут вступать в химическое взаимодействие с материалом футеровки и огнеупорных тиглей. Наиболее пригодны для данных сплавов футеровки из основных материалов: магнезита и хромомагнезита. При использовании кислых футеровок для плавки окисленной меди возможно оплавление футеровки из-за образования легкоплавких силикатов:
mCu2O + nSiO2 → mCu2O nSiO2.
При плавке бронз с повышенным содержанием свинца в печах с шамотной футеровкой может наблюдаться интенсивное разъедание огнеупоров за счет образования легкоплавких эвтектик (715 °С) в системе PbO–SiO2.
На практике для плавки меди и медных сплавов широко применяют графитошамотные плавильные тигли (смесь шамота с 30–40 % графита).
Для предохранения расплава от взаимодействия с газами печной атмосферы плавку необходимо вести быстро, целесообразно применять защитные покровы из древесного угля. Уголь должен быть тщательно просушен, а еще лучше прокален, для удаления адсорбированной влаги и продуктов сухой перегонки, в противном случае может произойти насыщение расплава водородом [1].
6.1.1. Раскисление меди и медных сплавов
Даже при плавке под защитными покровами и флюсами происходит частичное окисление меди. Кислород является нежелательной примесью в меди и медных сплавах, его необходимо удалить из расплава. Этот процесс называется раскислением. Раскисление осуществляют путем введения в расплав более активных к кислороду, чем медь, веществ – раскислителей, чтобы восстановить растворенную в расплаве закись меди. Раскислители могут быть разделены на две группы: поверхностные нерастворимые и объемные растворимые в металле.
К первой группе относятся: карбид кальция СаС2, борид магния Мg3B2, углерод и борный шлак B2O2 МgО. Процесс раскисления может быть описан следующими реакциями:
117
5Сu2O + СaС2 = СаО + 2СОг + 10Сu; 5Cu2О + Мg3B2 = 3МgО + B2O2 + 10Сu; 2Сu2О + С = СО2 + 4Сu;
Cu2O + B2O2 MgO = MgO B2O3 + 2Cu.
Реакции раскисления идут только на поверхности контакта расплава и раскислителей, поэтому процесс идет медленно. Для ускорения рекомендуется замешивать раскислители в расплав.
Преимуществом раскислителей первой группы является то, что они не переходят в расплав и не ухудшают качество металла.
Расход поверхностных раскислителей составляет 1–3 % от массы расплава.
К растворимым раскислителям относят:
1)раскислители, дающие газообразные продукты раскисления (водород, углеводороды и окись углерода);
2)раскислители, образующие парообразные или жидкие продукты раскисления (фосфор и литий);
3)раскислители, дающие твердые продукты раскисления (кальций, магний, алюминий, кремний, марганец).
Растворимые раскислители восстанавливают медь по всему объему расплава, поэтому процесс протекает значительно быстрее.
Восстановление окислов раскислителями 2-й и 3-й групп (R) может быть описано реакцией
[Сu2О] + [R] → (RО) + 2[Сu].
Вкачестве растворимых раскислителей чаще всего применяют фосфор, литий и бор. Они образуют продукты раскисления, которые легко удаляются из расплава. Следует иметь в виду, что избыток раскислителя остается в расплаве и может оказывать неблагоприятное воздействие на эксплуатационные свойства меди. Так, фосфор резко снижает электропроводность.
Влитейных цехах при плавке меди и сплавов, от которых не требуется высокая электропроводность, наибольшее распространение получило раскисление фосфором. Его вводят в расплав в виде
118
лигатуры медь–фосфор (8–12 % Р). При введении медно-фосфорной лигатуры возможно протекание следующих реакций:
5Cu2O + 2P → P2 O5 + 10Сu;
P2O5 + Cu2O →2CuPO3; 3Сu2О +Р → СuРО3 + 5Cu.
Фосфорно-кислая соль СuРО3 при температуре свыше 1000 °С находится в жидком состоянии и всплывает на поверхность расплава [1].
Для получения бескислородной меди, идущей на электротехнические цели, применяют вакуумный переплав, а при плавке в открытых печах производят так называемое дразнение. Для этого с поверхности расплава снимают шлак, засыпают слой прокаленного древесного угля и создают в печи восстановительную атмосферу (горение топлива с недостатком воздуха). В расплав погружают сырую древесину. Водяной пар и углеводороды – продукты сухой перегонки древесины – интенсивно перемешивают расплав, разбрызгивают медь, выбрасывая капли в восстановительную атмосферу. Восстановление меди протекает по следующим реакциям:
Сu2О +СH4 = СO2 +2H2O + 8Cu; Сu2О + СO4 = СO2 + 2Сu; 2Сu2O + С = СO2 + 4Сu; Сu2О + H2 = Н2О + 2Сu.
Содержание кислорода в твердой меди определяют металлографическим путем по площади, занимаемой эвтектикой Сu + Сu2O, или методом вакуум-плавления [12].
Наиболее простым способом проверки степени раскисленности меди является изучение характера и вида излома плоского слитка из выплавленного сплава. Окисленная медь легко ломается. В изломе имеет грубую кристаллическую структуру темно-красного (кирпичного) цвета. После раскисления медь приобретает большую пластичность. Излом становится мелкокристаллическим светло-
119
розового цвета. Сравнивая излом слитка с эталонами, можно по углу изгиба и цвету определить примерное остаточное содержание кислорода.
6.1.2. Рафинирование и дегазация медных сплавов
Меди и медные сплавы выплавляют с использованием различных покровов или защитных флюсов. Лучшим покровом считается прокаленный древесный уголь. Сгорая на поверхности расплава, уголь создает восстановительную атмосферу и тем самым уменьшает скорость окисления. Кроме того, уголь является хорошим поверхностным раскислителем. Преимуществом покрова из древесного угля является и легкость его удаления с расплава перед заливкой [17].
Для получения качественных отливок расплавы медных сплавов необходимо очистить от неметаллических включений и растворенного водорода.
Дегазацию медных расплавов осуществляют путем продувки азотом или инертными газами, вакуумированием и обработкой хлористыми солями.
Продувку газами ведут при температуре 1150–1200 °С в течение 5–10 мин и давлении газа 19,6–29,4 кПа.
Хлористые соли (МnСl2, ZnCl2, C2Cl6 и др.) вводят колокольчиком при 1150–1200 °С в количестве 0,1–0,22 % от массы расплава. Разливку сплава производят через 5–10 мин после обработки.
Вакуумирование ведут при остаточном давлении 0,66–1,3 кПа в течение 16–25 мин при температуре 1150–1300 °С. Нельзя вакуумировать сплавы, содержащие компоненты с высоким давлением пара, например цинк, чтобы избежать высоких потерь этих элементов.
Неметаллическими включениями чаще загрязнены сплавы, легированные легкоокисляющимися элементами, алюминием, титаном, бериллием и цирконием. Для очистки расплава от окислов этих элементов наиболее эффективна фильтрация через зернистые и жидкие фильтры, а также стеклоткань.
Для предотвращения загрязнения сплава газами и включениями плавку обычно ведут с применением покровов или флюсов. Наиболее часто используют покров из древесного угля, который сгорает
120
