
билет № (13)
.docx13. Галогеналканы. Электронное строение. Методы получения галогеналканов. Физические свойства. Реакции радикального замещения (реакция Вюрца и Вюрца-Гриньяра). Реакции элиминирования, правило Зайцева. Реакции нуклеофильного замещения - механизм, использование в органическом синтезе.
См билеты 11 и 12, здесь синтезы зайцева и вюрца
реакция Вюрца заключается в конденсации алкилгалогенидов под действием металлического Na, Li или реже K:
2RHal + 2Na ® R–R + 2NaHal.
Механизм реакции Вюрца состоит из двух основных стадий:
1) образование металлоорганического производного (если использется металл, а не заранее приготовленное металлоорганическое соединение):
RHal + 2Na ® R–Na + NaHal,
2) взаимодействие образовавшегося, в данном случае, натрийорганического соединения с другой молекулой алкилгалогенида:
RHal + R–Na ® RR + NaHal.
В зависимости от природы R и условий проведения реакции вторая стадия процесса может протекать по ионному либо по радикальному механизму.
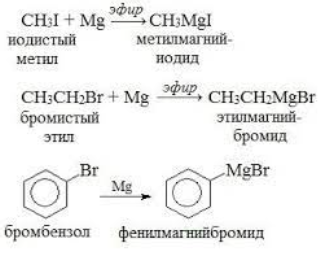
Реакция Гриньяра - металлорганическая химическая реакция, в которой арил- или алкилмагний_галогениды (также называемые реактивами Гриньяра ) действуют как нуклеофилы, атакуя электрофильный атом углерода с образованием углерод - углеродной связи. Реакция Гриньяра - важный метод создания углерод-углеродных связей, а также связей углерод-гетероатом (P,Sn,B,Si и др.)
Реакции элиминирования идут в соответствии с правилом Зайцева:
Отщепление атома водорода в реакциях дегидрогалогенирования и дегидратации происходит преимущественно от наименее гидрогенизированного атома углерода.
Реакция элиминирования (Е) для галогенводородов – отщепление протона и галоген-иона от атомов углерода с образованием кратной углерод-углеродной связи. • В связи с тем, что в процессе реакции от молекулы субстрата отщепляются атом водорода и галогена, то такие реакции называются дегидрогалогенированием.


