
6 курс / Кардиология / Практическая_электрокардиография_Марриотта_Galen_S_W_,_David_G_S
.pdfЭмфизема: болезнь легких, при которой разрушаются альвеолы, и легкие становятся огромного размера.
Torsades de pointes: вариант желудочковой тахикардии в результате увеличения времени восстановления желудочков. Французский термин используется для обозначения изменения - на правления комплекса QRS поочередно от положительного к отрицательному и обратно.
ССЫЛКИ
1.Cheng Z, Zhu K, Tian Z, et al. The findings of electrocardiography in patients with cardiac amyloidosis. Ann Noninvasive Electrocardiol. 2013;18(2):157162.
2.Bhardwaj R, Berzingi C, Miller C, et al. Differential diagnosis of acute pericarditis from normal variant early repolarization and left ventricular hypertrophy with early repolarization: an electrocardiographic study. Am J Med Sci. 2013;345(1):28-32.
3.Bruce MA, Spodick DH. Atypical electrocardiogram in acute pericarditis: characteristics and prevalence. J Electrocardiol. 1980;13:61-66.
4.Bashour FA, Cochran PA. The association of electrical alternans with pericardial effusion. Dis Chest. 1963;44:146.
5.Nizet PM, Marriott HJL. The electrocardiogram and pericardial effusion. JAMA. 1966;198:169.
6.Dalton JC, Pearson RJ, White PD. Constrictive pericarditis: a review and long term follow-up of 78 cases. Ann Intern Med. 1956;45:445.
7.Ferrari E, Imbert A, Chevalier T, et al. The ECG in pulmonary embolism. Predictive value of negative T waves in precordial leads - 80 case reports. Chest. 1997;111(3):537-543.
8.Wasserburger RH, Kelly JR, Rasmussen HK, et al. The electrocardiographic pentalogy of pulmonary emphysema: a correlation of roentgenographic findings and pulmonary function studies. Circulation. 1959;20:831-841.
9.Thomas AJ, Apiyasawat S, Spodick DH. Electrocardiographic detection of emphysema. Am J Cardiol. 2011;107(7):1090-1092.
10.Selvester RH, Rubin HB. New criteria for the electrocardiographic diagnosis of emphysema and cor pulmonale. Am Heart J. 1965;69:437-447.
11.Burch GE, Meyers R, Abildskov JA. A new electrocardiographic pattern observed in cerebrovascular accidents. Circulation. 1954;9:719.
12.Hersch C. Electrocardiographic changes in subarachnoid haemorrhage, meningitis, and intracranial spaceoccupying lesion. Br Heart J. 1964;26:785.
13.Surawicz B. Electrocardiographic pattern of cerebrovascular accident. JAMA. 1966; 197:913.
14.Shuster S. The electrocardiogram in subarachnoid haemorrhage. Br Heart J. 1960;22:316-320.
15.Fentz V, Gormsen J. Electrocardiographic patterns in patients with cerebrovascular accidents. Circulation. 1962;25:22-28.
16.Kono T, Morita H, Kuroiwa T. Left ventricular wall motion abnormalities in patients with subarachnoid hemorrhage: neurogenic stunned myocardium. J Am Coll Cardiol. 1994;24:636.
17.Wald DA. ECG manifestations of selected metabolic and endocrine disorders. Emerg Med Clin North Am. 2006;24(1):145-157.
18.Vanhaelst L, Neve P, Chailly P, et al. Coronary disease in hypothyroidism: observations in clinical myxoedema. Lancet. 1967;2:800-802.
19.Surawicz B, Mangiardi ML. Electrocardiogram in endocrine and metabolic disorders. Cardiovasc Clin. 1977;8:243-266.
20.Surawicz B, Mangiardi ML. Electrocardiogram in endocrine and metabolic disorders. In: Electrocardiographic Correlations. Philadelphia, PA: FA Davis; 1977:243-266.
21.Harumi K, Ouichi T. Q-T prolongation syndrome (in Japanese). In: Naika mook. Tokyo: Kinbara; 1981:210.
22.Okada M, Nishimura F, Yoshino H, et al. The J wave in accidental hypothermia. J Electrocardiol. 1983;16:23-28.
23.Frank S, Colliver JA, Frank A. The electrocardiogram in obesity: statistical analysis of 1,029 patients. J Am Coll Cardiol. 1986;7:295-299.
24.Starr JW, Wagner GW, Behar VS, et al. Vectorcardiographic criteria for the diagnosis of inferior myocardial infarction. Circulation. 1974;49:829-836.
25.Salerno DM, Asinger RW, Elsperger J, et al. Frequency of hypokalemia after successfully resuscitated out-of-hospital cardiac arrest compared with that in transmural acute myocardial infarction. Am J Cardiol. 1987;59:84-88.
26.Surawicz B. The interrelationship of electrolyte abnormalities and arrhythmias. In: Cardiac Arrhythmias: Their Mechanisms, Diagnosis, and Management. Philadelphia, PA: JB Lippincott; 1980:83.
27.Krikler DM, Curry PVL. Torsades de pointes, an atypical ventricular tachycardia. Br Heart J. 1976;38:117-120.
28.Surawicz B. Relationship between electrocardiogram and electrolytes. Am Heart J. 1967;73:814-
834.
29.Ettinger PO, Regan TJ, Oldewurtel HA. Hyperkalemia, cardiac conduction, and the electrocardiogram. A review. Am Heart J. 1974;88:360-371.
30.Sekiya S, Ichikawa S, Tsutsumi T, et al. Nonuniform action potential durations at different sites in canine left ventricle. Jpn Heart J. 1983;24:935-945.
31.Bashour TT. Spectrum of ventricular pacemaker exit block owing to hyperkalemia. Am J Cardiol. 1986;57:337-338.
32.Nirenburg DW, Ransil BJ. Q-aTc interval as a clinical indicator of hypercalcemia. Am J Cardiol. 1979;44:243-248.
33.Douglas PS, Carmichael KA, Palevsky PM. Extreme hypercalcemia and electrocardiographic changes. Am J Cardiol. 1984;54:674-679.
34.Sridharan MR, Horan LG. Electrocardiographic J wave in hypercalcemia. Am J Cardiol. 1984;54:672-673.
35.Vaughan Williams EM. Classification of antiarrhythmic drugs. In: Sandoe E, Flensted-Jensen E, Olsen KH, eds. Cardiac Arrhythmias. Sodertalje, Sweden: Astra; 1970:449-472.
36.Roden DM. Drug-induced prolongation of the QT interval. N Engl J Med. 2004;350:1013-1022.
37.Watanabe Y, Dreifus LS. Interactions of quinidine and potassium on atrioventricular transmission. Circ Res. 1967;20:434-446.

ГЛАВА 14 ВВЕДЕНИЕ В АРИТМИИ
Galen S. Wagner, David G. Strauss
ПОДХОД К ДИАГНОСТИКЕ АРИТМИЙ
Девять особенностей, которые должны быть исследованы при анализе каждой ЭКГ, представлены в Главе 3. Две из этих особенностей имеют первичное значение в оценке сердечного ритма:
1.Частота и регулярность.
2.Идентификация ритма.
Первоначально необходимо рассмотреть метод определения частоты и -ре гулярности ритмов. Нормальный синусовый ритм, с его лимитами в60-100 уд/мин и небольшой нерегулярностью в виде дыхательной аритмии, представлен в Главе 3. К первоначальным девяти особенностям, представленным в Главе 3, имеются дополнительные особенности ЭКГ, которые являются важными аспектами многих отклонений сердечного ритма:
1.Морфология зубца P;
2.Интервал PR;
3.Морфология комплекса QRS;
4.Интервал QTc.
Термин «аритмия» очень общий, относится ко всем ритмам, кроме регулярного синусового ритма. Даже небольшие колебания в частоте синусового ритма, вызванные изменением вегетативного баланса во время дыхательного цикла, называют «синусовой аритмией». Термин «дизритмия» был предложен некоторыми как альтернатива, но термин «аритмия» по-прежнему является более распространенным. Наличие аритмии не обязательно отражает кардиальное заболевание, так как широкий спектр неправильных ритмов обычно встречаются у здоровых лиц всех возрастов. Аритмии, прежде всего, классифицируются по их частоте, и обычно, у предсердий и желудочков имеется одинаковая частота. Однако среди аритмий есть много различных соотношений частоты предсердий и желудочков:

1.Предсердный и желудочковый ритмы связаны между собой и имеют одинаковую частоту, но (a) ритм генерируется в предсердиях или(b) ритм генерируется в желудочках.
2.Предсердный и желудочковый ритмы связаны между собой, но частота предсердий выше, чем частота желудочков (ритм исходит из предсердий).
3.Предсердный и желудочковые ритмы связаны между собой, но частота желудочков выше, чем частота предсердий (ритм исходит из желудочков).
4.Предсердный и желудочковый ритмы независимы друг от друга(атриовентрикулярная диссоциация и (a) предсердная и желудочковая частота одинаковы (изоритмическая диссоциация), (b) частота предсердий выше, чем частота желудочков, (c) частота желудочков выше, чем частота предсердий.
Когда предсердный и желудочковый ритмы связаны, но имеют различную частоту, ритм называют согласно частоте камеры(предсердие или желудочек), из которого он исходит(например, когда быстрый предсердный ритм связан с более медленной частотой желудочков, используется название «предсердная тахиаритмия»). Когда предсердный и желудочковый ритмы разобщены, названия даются обоим из ритмов(например, предсердная тахиаритмия с желудочковой тахиаритмией).
Термин брадиаритмия используется, чтобы идентифицировать любой ритм с ЧСС < 60 уд/мин, а «тахиаритмия» используется для идентификации любого ритма с ЧСС > 100 уд/мин. Есть также много аритмий, которые не изменяют ЧСС вне нормальных значений. В отличие от общих терминов «брадиаритмия» и «тахиаритмия», термины «брадикардия» и «тахикардия» относятся к вполне определенным аритмиям, таким как синусовая брадикардия и синусовая тахикардия. Два важных аспекта аритмий, которые являются основой для их понимания:
1.их механизм;
2.место их происхождения.
Механизмы, которые формируют аритмии:
1.проблемы формирования импульса (автоматизм);
2.проблемы проведения импульса (блокада или reentry).
ПРОБЛЕМЫ АВТОМАТИЗМА
Аритмии, вызванные проблемами автоматизма, могут сформироваться в любой клетке водителей ритма и проводящей системы, которая способна к спонтанной деполяризации. Такие клетки, которые называют клетками водителей ритма (пейсмекеров), присутствуют в:
1.Синусовый узел.
2.Клетки Пуркинье в предсердиях.
3.Общий пучок Гиса.
4.Правая и левая ножки пучка Гиса.
5.Клетки Пуркинье в ветвях и периферической желудочковой эндокардиальной сети.
См. Главу 1, рисунок 1.7.
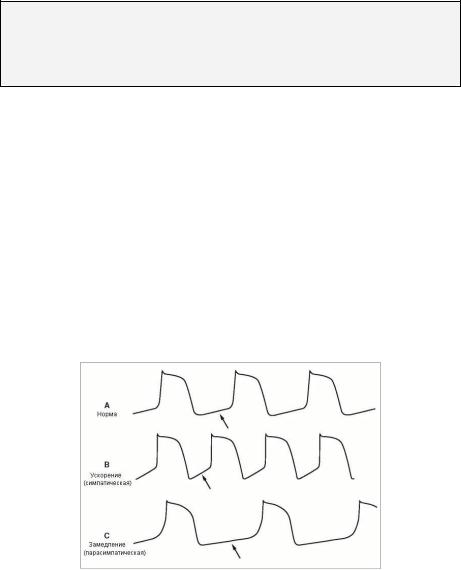
Обычно автоматизм синусового узла превышает автоматизм всех других частей пейсмекеров и проводящей системы, позволяя ему контролировать кардиальную частоту и ритм. Это важно из-за местоположения синусового узла и его взаимоотношений с парасимпатическим и симпатическим компонентами вегетативной нервной системы (см. Главу 3). Место ниже синусового узла может инициировать ритм сердца в результате ускорения его собственного автоматизма или в результате уменьшения автоматизма синусового узла. Термин «эктопический» часто применяется к ритмам, которые происходят из любого места, кроме синусового узла. Функция клеток пейсмекеров – формирование электрических импульсов, названных потенциалами действия, через процесс спонтанной деполяризации (Рис. 14.1). Когда автоматизма этих клеток ослабевает, может потребоваться применение искусственного водителя ритма (см. Главу 23). Ускорение автоматизма ограничено максимальной частотой формирования импульса в клетках пейсмекера и поэтому редко вызывает клинически важную тахиаритмию.
Рисунок 14.1. Схематические потенциалы действия пейсмекеров. А. Нормальный синусовый ритм. В. Усиление симпатической активности увеличивает наклон медленной спонтанной деполяризации, ускоряет ритм, как при синусовой тахикардии. С.
Усиление парасимпатической активности снижает наклон медленной спонтанной деполяризации, замедляет ритм, как при синусовой брадикардии. Стрелки указывают на спонтанную деполяризацию при всех трех состояниях.

Механизм, которым приводит к тахиаритмии, определяет направление лечения данной тахиаритмии. Ускоренный автоматизм можно лучше всего лечить, устранив причину его ускорения, а не занимаясь лечением самого ускорения. Когда ускоренный автоматизм исходит из синусового узла, причина усиления симпатической нервной активности кроется в одном из системных состояний, таких как физическая нагрузка, беспокойство, лихорадка, снижение сердечного выброса или тиреотоксикоз. Когда ускоренный автоматизм исходит из другого места, наиболее распространенными причинами являются дигиталисная интоксикация и ишемия. Поэтому ускоренный синусовый автоматизм контролируют путём воздействия на соответствующее системное состояние, а ускоренный несинусовый автоматизм, который называют «эктопическим», контролируют, купируя соответствующее состояние.
ПРОБЛЕМЫ ПРОВЕДЕНИЯ ИМПУЛЬСА: БЛОКАДЫ
Термин «блокада» используется по отношению к состояниям, которые замедляют или полностью нарушают проводимость(например, АВ-блокады; см. Главу 22), или блокады ножек пучка Гиса (см. Главу 6). Кардиальные импульсы могут быть частично заблокированы, вызывая задержку проведения (например, удлинение интервала PR), или полностью заблокированы, вызывая нарушение проводимости(например, полная АВ-блокада). При частичной блокаде импульсов нет никаких изменений в ЧСС, а при полной блокаде импульсов формируется брадиаритмия. Частичная или полная блокада может произойти в любом месте локализации пейсмекеров и проводящей системы (Таблица 14.1).
Таблица 14.1.
Блокады проведения импульсов
Место блокады |
Место первичного влияния |
||
1. Синусовый узел |
1. |
Миокард предсердий |
|
2. |
АВ-узел |
2. |
Пучок Гиса |
3. |
Пучок Гиса |
3. |
Ножки пучка Гиса |
4. |
Ножки пучка Гиса |
4. |
Миокард желудочков |
ПРОБЛЕМЫ ПРОВЕДЕНИЯ ИМПУЛЬСА: REENTRY
Хотя отклонения проводимости, достаточные для возникновения блокады, могут появиться только в рамках пейсмекеров и проводящей системы, неравная или неоднородная проводимость может встречаться в любой части сердца. Это неоднородное распространение электрических импульсов может привести к возвращению (reentry) импульса в область, которая была ранее депо-
1
ляризована и реполяризована. Reentry формирует циркулярное движение импульса, которое продолжается, пока импульс сталкивается с восприимчивыми клетками, приводя к одиночному преждевременному сокращению,
многократным преждевременным сокращениям, неустойчивой тахиаритмии
идаже устойчивой тахиаритмии. Есть три предпосылки к развитию reentry:
1.Наличие доступной цепи.
2.Различие в рефрактерных периодах двух проводящих путей в цепи.
3.Наличие достаточно медленной проводимости где-нибудь в цепи, чтобы позволить оставшейся части цепи возвратиться к состоянию нормальной реакции наим пульс.
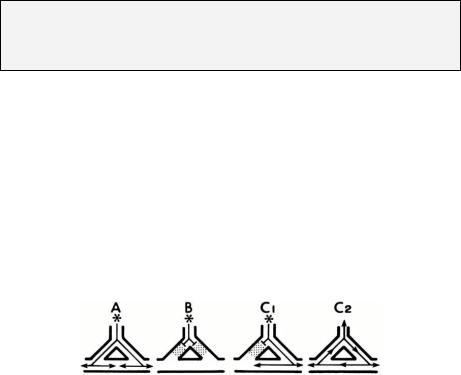
На рисунке 14.2 представлена диаграмма три различных ситуации восприимчивости проводящих путей к проведению импульса: (A) Оба проводящих пути восприимчивые – левый и правый пути закончили процесс восстановления и могут провести следующий импульс; (B) оба проводящих пути невосприимчивы - левый и правый путь все еще находятся в рефрактерном периоде и не могут провести следующий импульс; (C1) один проводящий путь восприимчив, а другой находится в рефрактерном периоде; (C2) левый проводящий путь невосприимчив, а правый путь может проводить импульс. К тому времени, когда импульс достигает дистального конца левого пути(проходя вниз по правому пути), левый путь выходит из состояния рефрактерности и может проводить импульс. Импульс продолжает свой путь по цепи reentry (ретроградно по левому пути), таким образом, формируя возвратную (реципрокную, reentrant) тахиаритмию.
Рисунок 14.2. Снежинки указывают на место формирования импульса, стрелки – направление проведения импульса, перпендикулярные линии – блокаду проведения импульса, затененная зона – область, которая ещё не закончила процесс реполяризации.
Пример возникновения «цепи reentry» в присутствии дополнительного проводящего АВ-пути представлен на рисунке14.3. Во время синусового ритма (см. Рис. 14.3A) у АВ-узла и пучка Кента было время, чтобы восстановиться после предыдущей активации. Преждевременное предсердное сокращение на рисунке 14.3B возникает в момент, когда пучок Кента ещё находится в рефрактерном периоде, а основной АВ-путь способен к проведению импульса (ситуация аналогична рисунку 14.2C1). Этот путь приводит к возникновению петли re-entry (см. Рис. 14.3C), аналогичной рисунку 14.2C2. Петля re-entry варьирует по размеру из ограниченной области в миокардиальных волокнах (см. Рис. 14.2C2) до охвата камер предсердий и желудочков (см. Рис. 14.3C).

Рисунок 14.3. Верх. Представлены пучок Кента между правым предсердием и правым желудочком и АВ-узел в области межжелудочковой перегородки. Х – место пейсмекера в синусовом узле (А) и правом предсердии (В). Отсутствует пейсмекер на рисунке С. Стрелки указывают на направление проведения импульса. Низ. Соответствующая ЭКГ показывает синусовый ритм с нормальным зубцомP перед комплексом QRS с желудочковым предвозбуждением (А); отрицательный зубец P перед комплексом QRS (предсердная экстрасистола) без предвозбуждения (В); и отрицательный зубец P перед комплексом QRS при реципрокной узловой тахикардии (С).
Термин микро-re-entry описывает механизм, который встречается, когда цепь re-entry слишком маленькая для активации, чтобы влиять на формирование всех зубцов ЭКГ. Импульсы, сформированные в пределах петлиreentry, распространяются через ближайший миокард так же, как бы они распространялись от автоматического или собственного водителя ритма. Зубцы P и комплексы QRS на ЭКГ формируются этим пассивным распространением активации через предсердия и желудочки. Микро-re-entry встречается в АВузле (см. Главу 18) и в желудочках (см. Главу 19).
Термин макро-re-entry описывает механизм, который встречается, когда цепь re-entry достаточно большая для активации, чтобы влиять на формирование всех зубцов ЭКГ (см. Рис. 14.3). Цикл активирующего импульса через правое предсердие (см. Рис. 14.3C) представлен частью зубца P, с оставшейся частью P, сформированной распространением импульса через выключенное левое предсердие. Цикл активирующего импульса через правый желудочек (см. Рис. 14.3C) представлен частью комплексаQRS, с оставшейся частью комплекса QRS, сформированной распространением импульса через выключенный левый желудочек.
Есть также формы макро-re-entry, в которых петля re-entry полностью находится в пределах миокарда предсердия или желудочка. Когда это происходит, дискретные зубцы P или комплексы QRS заменяются пилообразными или холмистыми волнами на ЭКГ (см. Главы 17 и 19).
Для правильного выбора терапии re-entry важно понимать механизм её возникновения. Чтобы любая петляre-entry могла существовать, необходимо, чтобы «голова» циркулирующего импульса не догоняла«хвост» рефрактер-
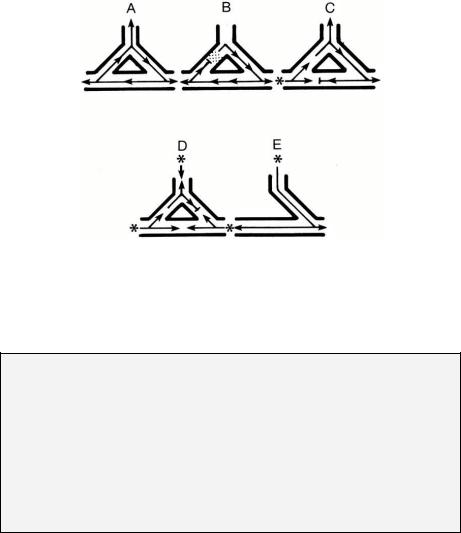
ного периода (Рис. 14.4A). Таким образом, всегда должен быть разрыв между «головой» и «хвостом» циркулирующего импульса. Устойчивая reentrant тахиаритмия может быть прервана:
Рисунок 14.4. Диаграмма с рисунка 14.2 использована для иллюстрации re-entry (А) и четырех механизмов ее прекращения(В-Е). Снежинки, стрелки, перпендикулярные линии и затененная зона имеют тоже значение, что и на рисунке 14.2. Снежинка на С указывает на место формирования эктопического импульса, три снежинки на D указывают на воздействие на все точки внешнего электрического тока при ЭИТ, и одиночная снежинка на E указывает на формирование синусового импульса.
1.Применение препаратов, которые ускоряют проведение импульсов в цепи re-entry так, чтобы она столкнулась с областью, которая находится все ещё в рефрактерном периоде (см. Рис. 14.4B). Завершение тахиаритмии также происходит при использовании препаратов, увеличивающих рефрактерный период.
2.Использование импульса от искусственного электрокардиостимулятора, который деполяризует часть цепи re-entry, переводя её в рефрактерный период в момент возвращения циркулирующего импульса (см. Рис. 14.4C).
3.Использование прекардиальной кардиоверсии, которая охватывает все восприимчивые к импульсу части сердца, включая цепь re-entry, и формируя рефрактерный период к моменту возвращения циркулирующего импульса (см. Рис. 14.4D).
4.Хирургическая или катетерная абляция одного проводящего пути петлиre-entry. Например, абляция дополнительного АВ-пути у пациентов с желудочковым предвозбуждением (см. Рис. 14.4E).
КЛИНИЧЕСКИЕ МЕТОДЫ ОБНАРУЖЕНИЯ АРИТМИЙ
Внедрение палат наблюдения кардиальных пациентов в начале1960-х годов стимулировало быстрые достижения в диагностике и лечении аритмий. В этих палатах проводится непрерывный мониторинг пациентов, имеющих аритмии или высокий риск их развития при таких состояниях, как острый

инфаркт миокарда (см. Главу 2). Модифицированное грудное отведениеV1 (MCL1) обычно используется в качестве отведения для мониторирования, потому, что оно обеспечивает и хороший обзор предсердной активности, дифференцирование активности правого и левого желудочков(Рис. 14.5).2 Часто, однако, используется и мониторирование с большим количеством отведений, чтобы обеспечить более разнообразный обзор электрической активности сердца, и облегчить более быструю и точную интерпретацию ритма.
Рисунок 14.5. А. Синусовый ритм с БПНПГ и желудочковая экстрасистолия (4-ый комплекс с положительным QRS и 6-ой комплекс с отрицательнымQRS). В. Основной ритм – фибрилляция предсердий; с 4 по 7 комплексы имеют морфологию БНПГ.
ДИНАМИЧЕСКИЙ МОНИТОРИНГ (HOLTER)
Метод для непрерывного мониторирования ЭКГ амбулаторных пациентов в их обычной обстановке был разработан в 1960-х годах Holter3 и с тех пор нашёл широкое применение.3 Пациент через грудные электроды подключен к портативному записывающему устройству(рекордеру), которое записывает 1-3 отведения ЭКГ в течение24 часов. Пациент ведет дневник активности так, чтобы можно было скоррелировать симптомы пациента, его физическую активность и сердечный ритм. Таким образом, пациент мониторируется во время ситуаций, которые фактически происходят в реальных обстоятельствах. Холтеровское мониторирование используется, чтобы определить любую корреляцию между аритмией и симптомами, такими, как учащенное сердцебиение, головокружение, синкопе или боль в груди (Рис. 14.6).
Рисунок 14.6. Холтеровская запись в отведении MCL, захватывающая ЖЭ и ЖТ у 57-летнего мужчины с одышкой и сердцебиениями на фоне ОИМ.
